题目内容
5.在化学学科中经常使用下列物理量,其中跟阿伏加德罗常数(NA)无关的组合是( )①相对原子质量(Mr)
②摩尔质量(M)
③原子半径(r)
④溶解度(S)
⑤物质的量(n)
⑥溶质的质量分数(w)
⑦气体摩尔体积(Vm)
| A. | ①③④⑥ | B. | ②④⑤ | C. | ①②③④ | D. | ⑤⑥⑦ |
分析 根据物理量的定义以及单位,可以判断其与阿伏加德罗常数是否有关,相对原子质量,溶质的质量分数为具体数值,原子半径的单位为nm,溶解度的单位为g,这些物理量与阿伏加德罗常数均无关.
解答 解:①相对原子质量等于一个原子质量除以碳原子质量的$\frac{1}{12}$,和阿伏加德罗常数无关,故①符合;
②摩尔质量(g/mol)是单位物质的量物质的质量,与阿伏加德罗常数有关,故②不符合;
③原子半径是具体数据单位为nm;与阿伏加德罗常数无关,故③符合;
④溶解度是100g水中 达到饱和溶解溶质的质量,单位g,与阿伏加德罗常数无关;故④符合;
⑤物质的量是表示微观粒子数目多少的物理量;单位为mol,和阿伏加德罗常数有关,故⑤不符合;
⑥溶质的质量分数,是溶质质量除以溶液质量,与阿伏加德罗常数无关,故⑥符合;
⑦气体摩尔体积(L/mol)一定温度压强下1mol气体的体积,和阿伏加德罗常数有关,故⑦不符合;
故选A.
点评 本题考查了阿伏伽德罗常数的应用,理解各概念的含义和计算方法是解题关键,题目较简单.

练习册系列答案
相关题目
15.下列说法正确的是( )
| A. | NaCl与浓H2SO4加热可制HCl,推测NaI与浓H2SO4加热可制HI | |
| B. | SO2和SO3混合气体通入Ba(NO3)2溶液可得到BaSO3和BaSO4 | |
| C. | FeCl3能腐蚀Cu刻制印刷电路板,是因为铁比铜金属性强 | |
| D. | P的非金属性强于Si,H3PO4比H2SiO3的酸性强 |
16.NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 含有NA个氖原子的氖气在标准状况下的体积约为11.2 L | |
| B. | 30 g乙烷中含共用电子对总数为8NA | |
| C. | 常温常压下,11.2 L氮气所含的原子数目为NA | |
| D. | 常温下,0.05 mol CO2和SO2混合气体中所含氧原子数为0.1NA |
13.短周期主族元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为16,Z原子的最外层电子数等于其电子层数,Y与W处于同一主族,X的原子半径小于Y.下列说法正确的是( )
| A. | Z的氧化物属于碱性氧化物 | |
| B. | 原子半径:r(Y)<r(W)<r(Z) | |
| C. | W的简单气态氢化物的热稳定性比Y的强 | |
| D. | W的氧化物对应的水化物一定是强酸 |
20.下列物质在变化过程中,化学键没有被破坏的是( )
| A. | 干冰升华 | B. | 食盐溶解 | ||
| C. | 氯化铵受热,固体消失 | D. | 电解水 |
10.用NA表示阿伏加德罗常数的值,下列说法均不正确的是( )
①将1mol氯气通入一定量水中发生反应转移电子数为NA
②12.0g熔融的NaHSO4中含有的阳离子数为0.1NA
③在标准状况下,22.4L辛烷中的分子数为NA
④1mol羟基中含有的电子数为10NA
⑤1mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA.
①将1mol氯气通入一定量水中发生反应转移电子数为NA
②12.0g熔融的NaHSO4中含有的阳离子数为0.1NA
③在标准状况下,22.4L辛烷中的分子数为NA
④1mol羟基中含有的电子数为10NA
⑤1mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA.
| A. | ②③⑤ | B. | ①②④ | C. | ①③④ | D. | ③④⑤ |
17.有机物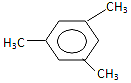 用系统命名法命名的名称为( )
用系统命名法命名的名称为( )
 用系统命名法命名的名称为( )
用系统命名法命名的名称为( )| A. | 间三甲苯 | B. | 1,3,5-三甲苯 | C. | 三甲苯 | D. | 1-3-5,三甲苯 |
14.将amolH2、Cl2混合气体(体积比为1:2)经光照充分反应后,所得气体恰好使溶液中bmolNaOH完全转变为盐,则a、b的关系为( )
| A. | a=b | B. | 2a=b | C. | 4a=3b | D. | 2a=3b |
 如图所示的装置,C、D、E、F、X、Y都是惰性电极.将直流电源接通后,向(乙)中滴入酚酞荣特,在F极附近呈红色.
如图所示的装置,C、D、E、F、X、Y都是惰性电极.将直流电源接通后,向(乙)中滴入酚酞荣特,在F极附近呈红色.