题目内容
【题目】某校课外活动小组为了探究铜与稀硝酸反应产生的是NO气体,设计了如下实验。实验装置如图所示:
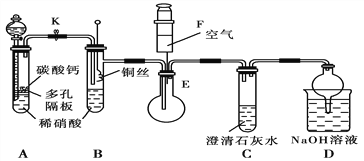
(1)设计装置A的目的是_______________________________________________ ,A中反应的化学方程式是__________________________________________
(2)在(1)中的操作后将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现象是_________________________________________;B中反应的离子方程式是________________________________________。
(3)装置E和F的作用是_____________________________________;为实现此目的,操作方法是_______________________。
【答案】 利用生成的二氧化碳将整个装置内的空气赶尽,避免NO和氧气反应生成二氧化氮对气体产物的观察产生干扰 CaCO3+2HNO3=Ca(NO3)2+CO2↑+H2O 铜丝表面产生气泡,稀硝酸液面上仍为无色,溶液变为蓝色 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O 验证无色气体为NO 将注射器F中的空气推入E中(或将E中的无色气体吸入到注射器中)
【解析】(1)因烧瓶中有空气,则生成的NO能与氧气反应生成二氧化氮,利用A装置生成二氧化碳将整个装置内的空气赶尽,避免NO和氧气反应生成二氧化氮对气体产物的观察产生干扰;为达到此目的,应进行的操作是观察到C中变浑浊,关闭K,移动铜丝与硝酸接触;A中稀硝酸和碳酸钙反应生成硝酸钙、二氧化碳和水,反应的化学方程式是:CaCO3+2HNO3=Ca(NO3)2+CO2↑+H2O;
(2)因铜与稀硝酸反应生成硝酸铜、NO和水,其离子反应为3Cu+2NO3-+8H+═3Cu2++2NO↑+4H2O,观察到气泡冒出和溶液变为蓝色;
(3)将F中的空气推入E中,发生反应2NO+O2=2NO2,E中无色气体变为红棕色,证明NO存在,则装置E和F的作用是验证NO的生成。

 一本好题口算题卡系列答案
一本好题口算题卡系列答案