题目内容
8. 某同学在实验室完成以下实验:
某同学在实验室完成以下实验:(1)证明溴乙烷在NaOH水溶液中发生了取代反应,下列方案可行的是C(填字母)
a.对反应产物进行分离提纯后,利用红外光谱法检测是否含有乙醇
b.取反应后的水溶液,向其中加入AgNO3溶液,检验是否存在Br-
c.取反应后的水溶液,向其中加入稀硝酸至溶液呈酸性,再加入AgNO3溶液,检验是否存在Br-
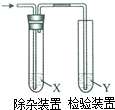
(2)利用以下装置检验乙烯
①若用溴乙烷与NaOH乙醇溶液共热制取乙烯,请写出该反应的化学方程式CH3CH2Br+NaOH $→_{△}^{醇}$CH2=CH2↑+NaBr+H2O,反应类型为消去反应.若Y中的试剂为酸性KMnO4溶液,干扰乙烯检验的杂质为乙醇,X中的试剂为水.
②若用乙醇与浓硫酸共热制取乙烯,请写出该反应的化学方程式CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O,X、Y中试剂分别为氢氧化钠溶液,溴水.
分析 (1)无论发生取代反应还是消去反应,溶液中都会产生Br-,但生成的有机物不同,故应检验生成的有机物;
(2)溴乙烷与NaOH的乙醇溶液共热,发生消去反应生成乙烯;利用溴乙烷和NaOH的乙醇溶液共热制备乙烯时,乙烯中可能混有溴乙烷、乙醇、水蒸气等杂质,乙醇也能使高锰酸钾酸性溶液褪色,应先将气体通入水中以除去乙醇;
(3)乙醇在浓硫酸作用下加热到170°C生成乙烯和水;用乙醇与浓硫酸共热制取乙烯,乙烯中混有的二氧化硫也能使高锰酸钾酸性溶液褪色,故检验乙烯前必须通过氢氧化钠溶液将二氧化硫除去.
解答 解:(1)溴乙烷在NaOH水溶液中发生了取代反应生成乙醇与溴化钠,发生消去反应生成乙烯和溴化钠,可以对反应产物进行分离提纯后,利用红外光谱法检测是否含有乙醇,故选A;
(2)溴乙烷与NaOH的乙醇溶液共热,发生消去反应,反应方程式为:CH3CH2Br+NaOH $→_{△}^{醇}$CH2=CH2↑+NaBr+H2O;乙烯中混有的乙醇也能使高锰酸钾酸性溶液褪色,因此在检验乙烯时,应先将气体通入水中以除去乙醇,防止其对乙烯检验的干扰;
故答案为:CH3CH2Br+NaOH $→_{△}^{醇}$CH2=CH2↑+NaBr+H2O;乙醇;水;
(3)乙醇与浓硫酸混合加热到170℃发生消去反应生成乙烯,反应的化学方程式为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O;利用乙醇与浓硫酸共热制备乙烯时,乙烯中混有的二氧化硫也能使高锰酸钾酸性溶液褪色,故检验乙烯前必须通过氢氧化钠溶液将二氧化硫除去;
故答案为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O;氢氧化钠溶液;溴水.
点评 本题考查了物质的制备与检验,为高频考点,把握常见有机物的性质及反应类型为解答的关键,题目难度不大.

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案| A. | 葡萄糖 | B. | 麦芽糖 | C. | 蔗糖 | D. | 淀粉 |
| A. | 分子中可能含有一个醛基、一个羟基 | |
| B. | 分子中可能含有一个碳碳双键、两个羟基 | |
| C. | 六个碳原子可能连成环状 | |
| D. | 分子中可能含有一个羧基、一个碳碳双键 |
| A. | CH2=CH2和CH2=CHCH=CH2 | B. | CH3CH2Cl和CH2ClCH2CH2Cl | ||
| C. | C2H5OH和CH4O | D. | CH3COOH和C17H33COOH |
| A. | 升高温度,A2转化率增大 | |
| B. | 升高温度有利于速率增大,从而缩短达到平衡的时间 | |
| C. | 达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动 | |
| D. | 达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动 |
| A. | 质量数 | B. | 核外电子数 | C. | 核电荷数 | D. | 核内中子数 |
| A. | 蛋白质 | B. | 天然气 | C. | 聚乙烯 | D. | 葡萄糖 |
 ,该反应类型是加聚反应.
,该反应类型是加聚反应.