题目内容
为将反应2Al+6H+=2Al3++3H2↑的化学能转化为电能,下列装置能达到目的的是(铝条均已除去了氧化膜)( )。
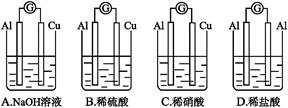

B
A、B、C三项中的装置均能将化学能转化为电能,A中反应为2Al+2OH-+2H2O=2Al +3H2↑,A项错误;B项符合题目的要求,正确;C项中反应为Al和硝酸反应生成NO,故C项达不到目的;D项中两电极全是Al,因而不能构成原电池,即不能将化学能转化为电能。
+3H2↑,A项错误;B项符合题目的要求,正确;C项中反应为Al和硝酸反应生成NO,故C项达不到目的;D项中两电极全是Al,因而不能构成原电池,即不能将化学能转化为电能。
 +3H2↑,A项错误;B项符合题目的要求,正确;C项中反应为Al和硝酸反应生成NO,故C项达不到目的;D项中两电极全是Al,因而不能构成原电池,即不能将化学能转化为电能。
+3H2↑,A项错误;B项符合题目的要求,正确;C项中反应为Al和硝酸反应生成NO,故C项达不到目的;D项中两电极全是Al,因而不能构成原电池,即不能将化学能转化为电能。
练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
 Al3+
Al3+

 O2+H2O+2e-=2OH-,
O2+H2O+2e-=2OH-,