题目内容
(13分)X、Y、Z、W、L、M六种短周期主族元素的原子序数依次增大,其中X、M的单质在常温下呈气态,Y的原子最外层电子数是其电子层数的2倍,Z 在同周期的主族元素中原子半径最大,W是地壳中含量最多的金属元素,L的单质晶体熔点高、硬度大,是一种重要的半导体材料。用化学用语回答下列问题:
在同周期的主族元素中原子半径最大,W是地壳中含量最多的金属元素,L的单质晶体熔点高、硬度大,是一种重要的半导体材料。用化学用语回答下列问题:
(1)L的元素符号为 ;M在元素周期表中的位置为 。
(2)Y、L、M的最高价含氧酸的酸性由弱到强的顺序是 。
(3)Y的最高价氧化物的电子式为 。原子序数比Y多2的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是 。
(4)Z、W各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为 。
(5)R与Y同周期,R的单质分子R2中有3个共价键,R与L能形成一 种新型无机非金属材料,其化学式是 。
种新型无机非金属材料,其化学式是 。
 在同周期的主族元素中原子半径最大,W是地壳中含量最多的金属元素,L的单质晶体熔点高、硬度大,是一种重要的半导体材料。用化学用语回答下列问题:
在同周期的主族元素中原子半径最大,W是地壳中含量最多的金属元素,L的单质晶体熔点高、硬度大,是一种重要的半导体材料。用化学用语回答下列问题:(1)L的元素符号为 ;M在元素周期表中的位置为 。
(2)Y、L、M的最高价含氧酸的酸性由弱到强的顺序是 。
(3)Y的最高价氧化物的电子式为 。原子序数比Y多2的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是 。
(4)Z、W各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为 。
(5)R与Y同周期,R的单质分子R2中有3个共价键,R与L能形成一
 种新型无机非金属材料,其化学式是 。
种新型无机非金属材料,其化学式是 。(13分)(1)Si(1分) 第三周期第ⅦA族(2分)
(2)H2SiO3 < H2CO3 < HClO4(2分)
(3)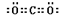 (2分) 2H2O2
(2分) 2H2O2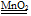 2H2O + O2↑(或其他合理答案)(2分)
2H2O + O2↑(或其他合理答案)(2分)
(4)Al(OH)3 + OH-=== AlO2-+ 2H2O (2分) (5)Si3N4 (2分)
(2)H2SiO3 < H2CO3 < HClO4(2分)
(3)
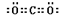 (2分) 2H2O2
(2分) 2H2O2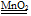 2H2O + O2↑(或其他合理答案)(2分)
2H2O + O2↑(或其他合理答案)(2分)(4)Al(OH)3 + OH-=== AlO2-+ 2H2O (2分) (5)Si3N4 (2分)
略

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
 -
-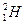 原子中的中子和质子
原子中的中子和质子 .1s22s22p63s23p2 B.1s22s22p3
.1s22s22p63s23p2 B.1s22s22p3