题目内容
地球的海水总量约有1.4×1018t,是人类最大的资源库。
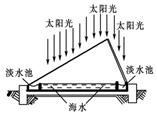
(1)如图利用海水得到淡水的方法为 。

(2)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如下图。a是电源的 极;Ⅰ口排出的是 (填“淡水” 或“浓水”)。

(3)海水淡化后的浓水中含大量盐分(主要含有Mg2+、Ca2+、Fe3+和SO42-),排入水中会改变水质,排到土壤中会导致土壤盐碱化,故不能直接排放,可以与氯碱工业联产。
电解前需要把浓水精制,所需试剂主要包括:HCl、NaOH、BaCl2、Na2CO3等),其中HCl的作用主要是 。
(4)铀是核反应最重要的燃料,其提炼技术直接关系着一个国家核工业或核武器的发展水平,海水中铀以UCl4形式存在(以离子形式存在),每吨海水只含3.3毫克铀,海水总量极大,铀总量相当巨大。不少国家正在探索海水提铀的方法。现在,已经研制成功一种螯合型离子交换树脂,它专门吸附海水中的铀,而不吸附其他元素。其反应原理为:___________________________(树脂用HR代替),发生离子交换后的离子交换膜用酸处理还可再生并得到含铀的溶液,其反应原理为:________________________。
(5)离子交换树脂法是制备纯水(去离子水) 的主要方法。某阳离子交换树酯的局部结构可写成(如图)。该阳离子交换树脂是由单体苯乙烯和交联剂对二乙烯基苯聚合后再经 反应得到的。自来水与该离子交换树脂交换作用后显 (填“酸性”、“碱性”或“中性”)。

(6)中国《生活用水卫生标准》中规定,水的总硬度不能过大。如果硬度过大,饮用后对人体健康与日常生活有一定影响。暂时硬水的硬度是由 (填阴离子符号)引起的,经 (填操作名称)后可被去掉。永久硬水的硬度可由离子交换法去掉。
(1)蒸馏法(1分)
(2)负(1分) 淡水(1分)
(3)除去过量的Na2CO3,并调节溶液的pH值(1分)
(4)4HR+U4+=UR4+4H+ UR4+4H+=4HR+U4+ (2分)
(5)磺化或取代(1分) 酸性(1分)(6)HCO3-(1分) 加热煮沸(1分)
【解析】
试题分析:(1)利用太阳能使水蒸发,为蒸馏法;
(2)a与阴极相连,为电源的负极;Ⅰ口排出的是电渗析法处理后的水,是淡水;
(3)HCl除掉过量的Na2CO3,调节溶液的pH值至中性;
(4)U4+替换HR中的H+,用酸处理时H+再替换U4+;
(5)磺酸基代替了苯环上的H,属于取代反应或磺化反应;自来水与该离子交换树脂交换作用后生成H+显酸性;
(6)暂时硬水的硬度是由HCO3-引起,加热煮沸生成沉淀而除去。
考点:本题考查海水的淡化、杂质的去除和有机反应类型。