��Ŀ����
��һ�ܱպ��ݵ������У����淴Ӧ3A(g) 3B(��)��C(��)�������仯��ͼ����ʾ�������ƽ����Է���������ʱ��ı仯��ͼ����ʾ��
3B(��)��C(��)�������仯��ͼ����ʾ�������ƽ����Է���������ʱ��ı仯��ͼ����ʾ��
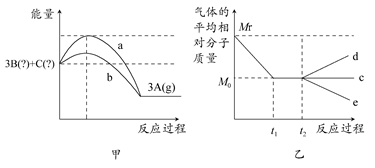
(1)��ͼ�����ж�3A(g) 3B(��)��C(��)������Ӧ��________��Ӧ(����ȡ����ȡ�)��ʵ��a��ʵ��b��Ƚϣ����������ķ�Ӧ������________��
3B(��)��C(��)������Ӧ��________��Ӧ(����ȡ����ȡ�)��ʵ��a��ʵ��b��Ƚϣ����������ķ�Ӧ������________��
(2)��ͼ�ҿ��Եó��й�B��C״̬�Ľ�����________��
����t2ʱ�������¶ȣ������ƽ����Է��������仯һ������________��(�c����d����e��)��
�����ı�ѹǿ�������ƽ����Է��������仯һ������c�ߣ���C���ʵ�״̬Ϊ________��
(3)���ƽ����¶Ȳ��䣬�������������һ������ƽ��ʱA��Ũ����ԭ����60%����B��________״̬��C��________״̬��
(4)���BΪ���壬CΪ���壬ȡ0.3 mol A��������1 L�����г�ַ�Ӧ��ƽ��ʱ���B��Ũ��Ϊ0.21 mol/L����ʹ��Ӧ���淴Ӧ��ʼ����ʼʱ�������м���0.3 mol B��ͬ�������£�Ҫʹƽ��ʱB��Ũ����Ϊ0.21 mol/L����C�����ʵ�����ȡֵ��ΧӦ����________��
 3B(��)��C(��)�������仯��ͼ����ʾ�������ƽ����Է���������ʱ��ı仯��ͼ����ʾ��
3B(��)��C(��)�������仯��ͼ����ʾ�������ƽ����Է���������ʱ��ı仯��ͼ����ʾ��
(1)��ͼ�����ж�3A(g)
 3B(��)��C(��)������Ӧ��________��Ӧ(����ȡ����ȡ�)��ʵ��a��ʵ��b��Ƚϣ����������ķ�Ӧ������________��
3B(��)��C(��)������Ӧ��________��Ӧ(����ȡ����ȡ�)��ʵ��a��ʵ��b��Ƚϣ����������ķ�Ӧ������________��(2)��ͼ�ҿ��Եó��й�B��C״̬�Ľ�����________��
����t2ʱ�������¶ȣ������ƽ����Է��������仯һ������________��(�c����d����e��)��
�����ı�ѹǿ�������ƽ����Է��������仯һ������c�ߣ���C���ʵ�״̬Ϊ________��
(3)���ƽ����¶Ȳ��䣬�������������һ������ƽ��ʱA��Ũ����ԭ����60%����B��________״̬��C��________״̬��
(4)���BΪ���壬CΪ���壬ȡ0.3 mol A��������1 L�����г�ַ�Ӧ��ƽ��ʱ���B��Ũ��Ϊ0.21 mol/L����ʹ��Ӧ���淴Ӧ��ʼ����ʼʱ�������м���0.3 mol B��ͬ�������£�Ҫʹƽ��ʱB��Ũ����Ϊ0.21 mol/L����C�����ʵ�����ȡֵ��ΧӦ����________��
(1)���ȣ�ʵ��b���˴�����(2)B��C��������һ��Ϊ���塡��e���ڷ���̬��(3)�����Һ�壻���� (4)n(C)>0.03 mol
ͼ���ǻ�ѧ��Ӧ�����������仯�Ĺ�ϵͼ����ȻB��C��������A�Ƿ��ȷ�Ӧ����3A(g) 3B(��)��C(��)����Ӧ�����ȷ�Ӧ��ʵ��b��Ӧ��Ҫ���������ͣ�����ʹ���˴�������ͼ�ҿ��Կ������ӷ�Ӧ��ʼ��ƽ��״̬����������ƽ����Է���������С�������ֿ��ܣ�һ������������������ˣ�B��C��Ϊ���壬һ�����������������ˣ�B����C��һ�������壬���ԣ�B��C��������һ��Ϊ���壬��t2ʱ�������¶ȣ�ƽ�������ƶ��������ƽ����Է���������С������ͼ��e�����ı�ѹǿ�������ƽ����Է����������䣬��÷�ӦΪһ�������������ķ�Ӧ��BΪ���壬CΪ�����塣���ƽ����¶Ȳ��䣬�������������һ������ƽ��ʱA��Ũ����ԭ����60%��˵��ƽ�������ƶ���������Ϊ������������ӵķ�Ӧ����BΪ�����壬CΪ���塣��Ϊ�Ǻ�������������Ҫʹƽ��ʱB��Ũ����ȣ�Ӧ�ü���ķ�Ӧ������൱��C�ǹ��壬ֻҪ�������з�Ӧ���輴�ɣ�ƽ��ʱC��Ӧ��0.03 mol������C�����ʵ���Ӧ�ô���0.03 mol��
3B(��)��C(��)����Ӧ�����ȷ�Ӧ��ʵ��b��Ӧ��Ҫ���������ͣ�����ʹ���˴�������ͼ�ҿ��Կ������ӷ�Ӧ��ʼ��ƽ��״̬����������ƽ����Է���������С�������ֿ��ܣ�һ������������������ˣ�B��C��Ϊ���壬һ�����������������ˣ�B����C��һ�������壬���ԣ�B��C��������һ��Ϊ���壬��t2ʱ�������¶ȣ�ƽ�������ƶ��������ƽ����Է���������С������ͼ��e�����ı�ѹǿ�������ƽ����Է����������䣬��÷�ӦΪһ�������������ķ�Ӧ��BΪ���壬CΪ�����塣���ƽ����¶Ȳ��䣬�������������һ������ƽ��ʱA��Ũ����ԭ����60%��˵��ƽ�������ƶ���������Ϊ������������ӵķ�Ӧ����BΪ�����壬CΪ���塣��Ϊ�Ǻ�������������Ҫʹƽ��ʱB��Ũ����ȣ�Ӧ�ü���ķ�Ӧ������൱��C�ǹ��壬ֻҪ�������з�Ӧ���輴�ɣ�ƽ��ʱC��Ӧ��0.03 mol������C�����ʵ���Ӧ�ô���0.03 mol��
 3B(��)��C(��)����Ӧ�����ȷ�Ӧ��ʵ��b��Ӧ��Ҫ���������ͣ�����ʹ���˴�������ͼ�ҿ��Կ������ӷ�Ӧ��ʼ��ƽ��״̬����������ƽ����Է���������С�������ֿ��ܣ�һ������������������ˣ�B��C��Ϊ���壬һ�����������������ˣ�B����C��һ�������壬���ԣ�B��C��������һ��Ϊ���壬��t2ʱ�������¶ȣ�ƽ�������ƶ��������ƽ����Է���������С������ͼ��e�����ı�ѹǿ�������ƽ����Է����������䣬��÷�ӦΪһ�������������ķ�Ӧ��BΪ���壬CΪ�����塣���ƽ����¶Ȳ��䣬�������������һ������ƽ��ʱA��Ũ����ԭ����60%��˵��ƽ�������ƶ���������Ϊ������������ӵķ�Ӧ����BΪ�����壬CΪ���塣��Ϊ�Ǻ�������������Ҫʹƽ��ʱB��Ũ����ȣ�Ӧ�ü���ķ�Ӧ������൱��C�ǹ��壬ֻҪ�������з�Ӧ���輴�ɣ�ƽ��ʱC��Ӧ��0.03 mol������C�����ʵ���Ӧ�ô���0.03 mol��
3B(��)��C(��)����Ӧ�����ȷ�Ӧ��ʵ��b��Ӧ��Ҫ���������ͣ�����ʹ���˴�������ͼ�ҿ��Կ������ӷ�Ӧ��ʼ��ƽ��״̬����������ƽ����Է���������С�������ֿ��ܣ�һ������������������ˣ�B��C��Ϊ���壬һ�����������������ˣ�B����C��һ�������壬���ԣ�B��C��������һ��Ϊ���壬��t2ʱ�������¶ȣ�ƽ�������ƶ��������ƽ����Է���������С������ͼ��e�����ı�ѹǿ�������ƽ����Է����������䣬��÷�ӦΪһ�������������ķ�Ӧ��BΪ���壬CΪ�����塣���ƽ����¶Ȳ��䣬�������������һ������ƽ��ʱA��Ũ����ԭ����60%��˵��ƽ�������ƶ���������Ϊ������������ӵķ�Ӧ����BΪ�����壬CΪ���塣��Ϊ�Ǻ�������������Ҫʹƽ��ʱB��Ũ����ȣ�Ӧ�ü���ķ�Ӧ������൱��C�ǹ��壬ֻҪ�������з�Ӧ���輴�ɣ�ƽ��ʱC��Ӧ��0.03 mol������C�����ʵ���Ӧ�ô���0.03 mol��
��ϰ��ϵ�д�
�����Ŀ
 C�ﵽƽ���B��ת������ѹǿ���¶ȵĹ�ϵ����ͼ,����˵����ȷ����( )
C�ﵽƽ���B��ת������ѹǿ���¶ȵĹ�ϵ����ͼ,����˵����ȷ����( )
 N2O4�Ŀ��淴Ӧ��,����״̬һ������ƽ��״̬����(����)
N2O4�Ŀ��淴Ӧ��,����״̬һ������ƽ��״̬����(����) 2C(g),��Ӧ�ﵽƽ��ʱ,�����������A��B�����ʵ���֮����C�����ʵ������,����ʱA��ת����Ϊ(����)��
2C(g),��Ӧ�ﵽƽ��ʱ,�����������A��B�����ʵ���֮����C�����ʵ������,����ʱA��ת����Ϊ(����)��
 CH3OH(g)��H2O(g)�����ܱ������£�����ʾ��ͼ��˵����Ӧ���е�t1ʱ��ʱ�ﵽƽ��״̬���� (����ĸ���)
CH3OH(g)��H2O(g)�����ܱ������£�����ʾ��ͼ��˵����Ӧ���е�t1ʱ��ʱ�ﵽƽ��״̬���� (����ĸ���)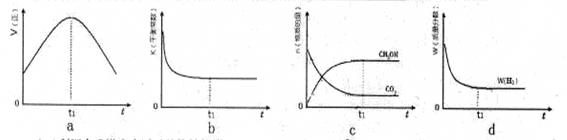
 2HBr(g)����H<0�����¶ȷֱ�ΪT1��T2��ƽ��ʱ��H2�����������Br2(g)�����ʵ����ı仯��ϵ��ͼ��ʾ������˵������ȷ���� (����)
2HBr(g)����H<0�����¶ȷֱ�ΪT1��T2��ƽ��ʱ��H2�����������Br2(g)�����ʵ����ı仯��ϵ��ͼ��ʾ������˵������ȷ���� (����)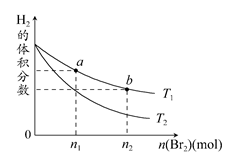
 2NH3(g)����H����92.2 kJ��mol��1���ϳɰ���ҵ��ԭ����N2�ɴӿ����з���õ���H2���ü����̿��ˮ������Ӧ�Ƶá�
2NH3(g)����H����92.2 kJ��mol��1���ϳɰ���ҵ��ԭ����N2�ɴӿ����з���õ���H2���ü����̿��ˮ������Ӧ�Ƶá�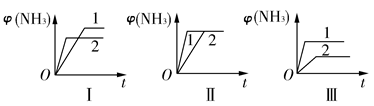

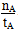 mol��L��1��min��1
mol��L��1��min��1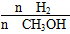 ����
���� 2C(g)�ﵽƽ��ı�־��(����)��
2C(g)�ﵽƽ��ı�־��(����)��