题目内容
12.据报道,在火星和金星大气层中发现了一种非常特殊的能导致温室效应的气态化合物,它的结构式为16O═C═18O.下列说法正确的是( )| A. | 16O与18O为同种核素 | |
| B. | 16O═C═18O与16O═C═16O互为同位素 | |
| C. | 16O═C═18O与16O═C═16O的化学性质几乎完全相同 | |
| D. | 目前提出的“低碳经济”的目标是向空气中增加CO2,促进碳的平衡 |
分析 A.原子的质子数相同、但中子数不同,则为同种元素的不同核素;
B.质子数相同、但中子数不同的原子互为同位素;
C.物质相同,则化学性质相同;
D.根据减少含碳物质的排放来控制温室效应.
解答 解:A.16O与18O的质子数都是8,但中子数分别为8、10,则都是氧元素的不同核素,故A错误;
B.16O=C=18O与16O=C=16O为化合物,而质子数相同、但中子数不同的原子互为同位素,故B错误;
C.16O=C=18O与16O=C=16O为组成元素完全相同,结构相同的同种物质,则化学性质相同,故C正确;
D.由信息可知,提出的“零碳经济”是要减少含碳物质的排放,则不再向环境排放CO2,有利于控制温室效应,故D错误;
故选C.
点评 本题属于信息习题,较简单,学生只要学会利用信息结合所学知识即可解答,明确核素、同位素、温室效应等概念是解答本题的关键.

练习册系列答案
相关题目
3.化学与生活密切相关,下列说法不正确的是( )
| A. | 硅太阳能电池板在工作时,可以将化学能转化为电能 | |
| B. | 用纯碱溶液可洗涤餐具上的油污 | |
| C. | 用灼烧并闻气味的方法可区别真丝织物和人造棉 | |
| D. | 水陆两用公共汽车中,用于密封的橡胶材料是高分子化合物 |
20.关于HOOC-CH═CH-CH2OH,下列说法不正确的是( )
| A. | 分子式为C4H6O3,每摩尔该物质充分燃烧需消耗4mol O2 | |
| B. | 能发生取代、加成、氧化、加聚、中和等反应 | |
| C. | 分别与足量Na、NaOH、Na2CO3反应,生成物均为NaOOC-CH═CH-CH2OH | |
| D. | 该分子含有两种官能团 |
7.室温下,下列叙述正确的是( )
| A. | 将一定量的醋酸与一定量的NaOH溶液混合,若混合后溶液中存在:c(CH3COO-)+c(CH3COOH)=2c(Na+)等式,则也一定存在c(OH-)+c(CH3COO-)=c(CH3COOH)+c(H+) | |
| B. | 等浓度、等体积的Na2CO3溶液和NaHCO3溶液混合:$\frac{c(HC{{O}_{3}}^{-})}{c({H}_{2}C{O}_{3})}<\frac{c(C{{O}_{3}}^{2-})}{c(HC{{O}_{3}}^{-})}$ | |
| C. | 常温下,V1 L pH=11的溶液与V2 L pH=3的HA溶液混合后显中性,则V1≥V2 | |
| D. | 已知A-+H2B(过量)=HA+HB-,则酸性强弱顺序一定为:HB-<HA<H2B |
17.无水氯化铝在生产、生活中应用广泛.
(1)氯化铝在水中形成具有净水作用的氢氧化铝胶体,其反应的离子方程式为Al3++3H2O?Al(OH)3+3H+.
(2)工业上用铝土矿(主要成分为Al2O3,含有Fe2O3、SiO2等杂质)制取无水氯化铝的一种工艺流程示意如下:
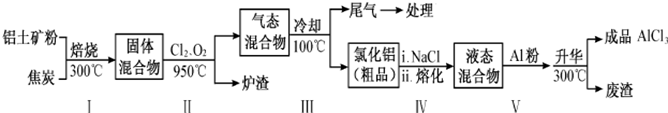
已知:
①步骤Ⅰ中焙烧使固体水分挥发、气孔数目增多,其作用是防止后续步骤生成的AlCl3水解或增大反应物的接触面积,加快反应速率(只要求写出一种).
②步骤Ⅱ中若不通入氯气和氧气,则反应生成相对原子质量比硅大的单质是Fe或铁.
③已知:
Al2O3(s)+3C(s)=2Al(s)+3CO(g)△H1=+1344.1kJ•mol-1
2AlCl3(g)=2Al(s)+3Cl2(g)△H2=+1169.2kJ•mol-1
由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为Al2O3(s)+3C(s)+3Cl2(g)=2AlCl3(g))+3CO(g)△H=+174.9KJ/mol.
④步骤Ⅲ的经冷却至室温后,气体用足量的NaOH冷溶液吸收,生成的盐主要有3种,其化学式分别为NaCl、NaClO、Na2CO3 .
⑤结合流程及相关数据分析,步骤Ⅴ中加入铝粉的目的是除去FeCl3,提高AlCl3纯度.
(1)氯化铝在水中形成具有净水作用的氢氧化铝胶体,其反应的离子方程式为Al3++3H2O?Al(OH)3+3H+.
(2)工业上用铝土矿(主要成分为Al2O3,含有Fe2O3、SiO2等杂质)制取无水氯化铝的一种工艺流程示意如下:

已知:
| 物质 | SiCl4 | AlCl3 | FeCl3 | FeCl2 |
| 沸点/℃ | 57.6 | 180(升华) | 300(升华) | 1023 |
②步骤Ⅱ中若不通入氯气和氧气,则反应生成相对原子质量比硅大的单质是Fe或铁.
③已知:
Al2O3(s)+3C(s)=2Al(s)+3CO(g)△H1=+1344.1kJ•mol-1
2AlCl3(g)=2Al(s)+3Cl2(g)△H2=+1169.2kJ•mol-1
由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为Al2O3(s)+3C(s)+3Cl2(g)=2AlCl3(g))+3CO(g)△H=+174.9KJ/mol.
④步骤Ⅲ的经冷却至室温后,气体用足量的NaOH冷溶液吸收,生成的盐主要有3种,其化学式分别为NaCl、NaClO、Na2CO3 .
⑤结合流程及相关数据分析,步骤Ⅴ中加入铝粉的目的是除去FeCl3,提高AlCl3纯度.
4.下列离子中半径最大的是( )
| A. | Na+ | B. | Mg2+ | C. | O2- | D. | F- |
1.下列有关海水综合利用的说法正确的是( )
| A. | 电解饱和食盐水可制得金属钠 | B. | 海带提碘只涉及物理变化 | ||
| C. | 海水提溴涉及到氧化还原反应 | D. | 海水提镁涉及到复分解反应 |

 ,水杨酸酯E为紫外吸收剂,可用于配制防晒霜.E的一种合成路线如下:
,水杨酸酯E为紫外吸收剂,可用于配制防晒霜.E的一种合成路线如下:
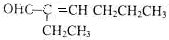 ;若只能一次取样,请提出检验C中2种官能团的简要方案:用银氨溶液先检验醛基,再加稀盐酸使溶液呈酸性后,加溴水检验碳碳双键;
;若只能一次取样,请提出检验C中2种官能团的简要方案:用银氨溶液先检验醛基,再加稀盐酸使溶液呈酸性后,加溴水检验碳碳双键; 、HOCH2CH2C≡C-C≡C-COOH、
、HOCH2CH2C≡C-C≡C-COOH、 ;
; :
: