题目内容
(15分)云南省曲靖的铬渣污染经媒体报道后,铬污染再次引起人们的关注。利用化学原理可以对工厂排放的含铬废水、铬渣等进行有效处理。
I.含铬废水的处理:某企业排放的含铬废水中含有较多毒性较大的Cr2O72-,某研究性学习小组为了变废为宝,将废水处理得到金属铬,设计了如下的工艺流程。

(1)加酸调节到pH=6,则用pH试纸测定溶液pH的操作是: 。
。
(2)在含Cr2O72-废水中存在着平衡:Cr2O72-+H2O 2CrO42-+2H+,请写出该平衡的平衡常数表达式k= ,若继续加水稀释,平衡将 移动(填“正向”、“逆向”“不”)。
2CrO42-+2H+,请写出该平衡的平衡常数表达式k= ,若继续加水稀释,平衡将 移动(填“正向”、“逆向”“不”)。
(3)请写出通入SO2时发生的离子反应: 。
(4)写出加入铝粒时发生反应的化学方程式 ,该反应是焓 (填“增加”或“减少”)反应。
II.铬渣的处理
铬渣烧结炼铁法:铬渣中约含有55%的氧化钙和氧化镁,此外还含有15%左右的氧化铁,这些都是炼铁所需的成份。少量的铬渣代替消石灰同铁矿粉、煤粉混合,经烧结后送入高炉冶炼,六价铬还原为三价铬或金属铬,金属铬熔入铁水,而其它成分熔入熔渣。炼铁可使铬渣彻底解毒并充分利用,是铬渣治理的良好方法之一。
碱性溶液还原法:直接在碱性铬渣中加入硫化钠等进行六价铬的还原反应,形成Cr(OH)3沉淀后,过滤回收铬污泥。
(5)铬渣烧结炼铁法中煤粉的作用是 。(写两点)
(6)请配平碱性溶液还原法中发生的离子反应:□Cr2O72-+□S2—+□H2O=□Cr(OH)3+□S2O32—+□OH—
I.含铬废水的处理:某企业排放的含铬废水中含有较多毒性较大的Cr2O72-,某研究性学习小组为了变废为宝,将废水处理得到金属铬,设计了如下的工艺流程。

(1)加酸调节到pH=6,则用pH试纸测定溶液pH的操作是:
 。
。(2)在含Cr2O72-废水中存在着平衡:Cr2O72-+H2O
 2CrO42-+2H+,请写出该平衡的平衡常数表达式k= ,若继续加水稀释,平衡将 移动(填“正向”、“逆向”“不”)。
2CrO42-+2H+,请写出该平衡的平衡常数表达式k= ,若继续加水稀释,平衡将 移动(填“正向”、“逆向”“不”)。(3)请写出通入SO2时发生的离子反应: 。
(4)写出加入铝粒时发生反应的化学方程式 ,该反应是焓 (填“增加”或“减少”)反应。
II.铬渣的处理
铬渣烧结炼铁法:铬渣中约含有55%的氧化钙和氧化镁,此外还含有15%左右的氧化铁,这些都是炼铁所需的成份。少量的铬渣代替消石灰同铁矿粉、煤粉混合,经烧结后送入高炉冶炼,六价铬还原为三价铬或金属铬,金属铬熔入铁水,而其它成分熔入熔渣。炼铁可使铬渣彻底解毒并充分利用,是铬渣治理的良好方法之一。
碱性溶液还原法:直接在碱性铬渣中加入硫化钠等进行六价铬的还原反应,形成Cr(OH)3沉淀后,过滤回收铬污泥。
(5)铬渣烧结炼铁法中煤粉的作用是 。(写两点)
(6)请配平碱性溶液还原法中发生的离子反应:□Cr2O72-+□S2—+□H2O=□Cr(OH)3+□S2O32—+□OH—
(1)将一小块pH试纸放在表面皿上,用玻璃棒蘸取少量待测液,点在pH试纸上,再与标准比色卡对照。(2分)
(2)c(CrO42-)2c(H+)2/c(Cr2O72-)(2分) 正向(2分)
(3)Cr2O72-+3SO2+2H+=2Cr3++3SO42-+ H2O(2分)
(4)2Al+Cr2O3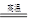 Al2O3+2Cr(2分) 焓减少(1分)
Al2O3+2Cr(2分) 焓减少(1分)
(5)为高炉冶炼过程提供热源;燃烧后生成的CO是高炉冶炼过程的还原剂;还起到高温填料的作用(写两点即可)(2分)
(6)4 6 19 8 3 14 (2分)
(2)c(CrO42-)2c(H+)2/c(Cr2O72-)(2分) 正向(2分)
(3)Cr2O72-+3SO2+2H+=2Cr3++3SO42-+ H2O(2分)
(4)2Al+Cr2O3
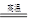 Al2O3+2Cr(2分) 焓减少(1分)
Al2O3+2Cr(2分) 焓减少(1分)(5)为高炉冶炼过程提供热源;燃烧后生成的CO是高炉冶炼过程的还原剂;还起到高温填料的作用(写两点即可)(2分)
(6)4 6 19 8 3 14 (2分)
(1)测定溶液的pH的方法是:用玻璃棒蘸取待测溶液滴在pH试纸的中心位置,然后对照标准比色卡,读出对应颜色的数据。
(2)水为纯液体,浓度为常数,在平衡常数表达式中不出现;加水稀释,使c(Cr2O72-)、c(CrO42-)、c(H+)均减少,该反应的浓度商公式中,分子减少的更快,使浓度商<平衡常数,平衡正向移动。
(3)根据流程图分析Cr2O72-转化为Cr3+,SO2一般是转化为SO42-,根据化合价升降法配平方程式。
(4)铝热反应是放热反应,即焓减少反应。
(6)根据化合价升降法配平方程式。
(2)水为纯液体,浓度为常数,在平衡常数表达式中不出现;加水稀释,使c(Cr2O72-)、c(CrO42-)、c(H+)均减少,该反应的浓度商公式中,分子减少的更快,使浓度商<平衡常数,平衡正向移动。
(3)根据流程图分析Cr2O72-转化为Cr3+,SO2一般是转化为SO42-,根据化合价升降法配平方程式。
(4)铝热反应是放热反应,即焓减少反应。
(6)根据化合价升降法配平方程式。

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目