题目内容
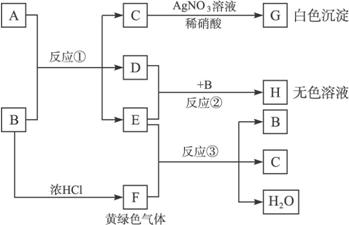
已知:A、B 是两种盐的溶液,其焰色反应均呈黄色,A 呈中性,B呈碱性并具有氧化性;D 在CCl4中呈紫红色。下图为相关实验步骤和实验现象
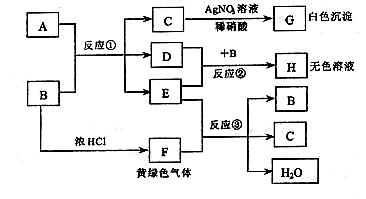
请回答:
(1) 依次写出 A、B 中溶质的化学式:A_______ B________
(2) 依次写出反应①和②的离子方程式(H 中含有某+5价元素含氧酸根离子)
______________________________ ; ___________________________
(3) 写出反应③的化学方程式___________________________________
⑴ NaI NaClO ⑵ 2I-+ClO-+H2O=I2+Cl-+2OH— I2+5ClO-+2OH_=2IO3-+5Cl-+H2O ⑶ Cl2+2NaOH=NaClO+NaCl+H2O
解析:
本题是典型的无机推断题,主要考查学生对元素化合物的综合应用能力,属较难题。本题突破口为:1 A、B焰色反应均呈黄色知A、B含Na元素;2B呈碱性并具有氧化性可推知B可能为NaOH或对应弱酸盐,具有氧化性可推知B为NaClO;3 D 在CCl4中呈紫红色,可得D为I2,则A中有I元素,A为NaI。突破口突破之后再由其他条件推断对应的物质。

练习册系列答案
相关题目


 (2011?德州二模)已知两个羟基同时连在同一碳原子上的结构是不稳定的,它要发生脱水反应:
(2011?德州二模)已知两个羟基同时连在同一碳原子上的结构是不稳定的,它要发生脱水反应: