题目内容
(12分) Ba2+是一种重金属离子,有一环境监测小组欲利用Na2S2O3、KI、K2Cr2O7等试剂测定某工厂废水中Ba2+的浓度。
(1)现需配制250mL0.100mol·L-1的标准Na2S2O3溶液,所需要的玻璃仪器除量筒、烧杯、玻璃棒外,还需要 ▲ 。
(2)配制上述溶液需准确称取Na2S2O3固体的质量为 ▲ g。
(3)另取废水40.00mL,控制适当的酸度,加入足量的K2Cr2O7溶液,得BaCrO4沉淀,沉淀经洗涤、过滤后,用适量的稀盐酸溶解,此时CrO全部转化为Cr2O;再加入过量KI溶液进行反应,然后在反应溶液中再滴加上述Na2S2O3溶液,反应完全时,消耗Na2S2O3溶液24.00mL。已知有关反应的离子方程式为:①Cr2O+6I-+14H+==2Cr3++3I2+7H2O;②I2+2S2O===2I-+S4O。试计算该工厂废水中Ba2+的物质的量浓度为多少?
(1)胶头滴管、250mL容量瓶(2分)
(2)4.0 (4分) (3)0.020mol·L-1(含过程共6分)
(3)设Ba2+的物质的量为x,则根据相关反应可得以下关系式:
Ba2+~BaCrO4~1/2Cr2O~3/2I2~3S2O
1 3
x 0.024L×0.100mol·L-1
解得:x=8.0×10-4mol,故
c(Ba2+)=8.0×10-4mol÷0.040L=0.020mol·L-1。
解析:略

.(12分) 现有A、B、C、D、E五种可溶性强电解质,它们在水中可电离产
生下列离子(各种离子不重复)。
| 阳离子 | H+、Na+、A13+、Ag+、Ba2+ |
| 阴离子 | OH-、C1-、CO32-、NO3-、SO42- |
已知:①A、B两溶液呈碱性,C、D、E溶液呈酸性;常温下,0.1 mol/L
B溶液的pH大于13,0.1 mol/L C溶液的pH等于1
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有
气体产生;(沉淀包括难溶物和微溶物,下同)。
③D溶液与另外四种溶液反应都能产生沉淀。
试回答下列问题:
(1)写出A、B、C、D、E的化学式:A、 B、
C、 D、 E
(2)写出A、E溶液反应的离子方程式:
。
(3)写出B溶液与C溶液恰好完全反应的离子方程式:
_____ 。
(4)将C溶液逐滴加入等体积、等物质量的浓度的A溶液中,反应后溶液中各种离子浓度由小到大的顺序为(带两个单位电荷的离子不参与比较):__________________________________。
.(12分) 现有A、B、C、D、E五种可溶性强电解质,它们在水中可电离产
生下列离子(各种离子不重复)。
|
阳离子 |
H+、Na+、A13+、Ag+、Ba2+ |
|
阴离子 |
OH-、C1-、CO32-、NO3-、SO42- |
已知:①A、B两溶液呈碱性,C、D、E溶液呈酸性;常温下,0.1 mol/L
B溶液的pH大于13,0.1 mol/L C溶液的pH等于1
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有
气体产生;(沉淀包括难溶物和微溶物,下同)。
③D溶液与另外四种溶液反应都能产生沉淀。
试回答下列问题:
(1)写出A、B、C、D、E的化学式:A、 B、
C、 D、 E
(2)写出A、E溶液反应的离子方程式:
。
(3)写出B溶液与C溶液恰好完全反应的离子方程式:
_____ 。
(4)将C溶液逐滴加入等体积、等物质量的浓度的A溶液中,反应后溶液中各种离子浓度由小到大的顺序为(带两个单位电荷的离子不参与比较):__________________________________。
(12分)甲、乙、丙、丁四种物质均为下列离子组成的可溶性化合物,组成这四种物质的离子(离子不能重复组合)有:
|
阳离子 |
Ag+、Mg2+、Al3+、Ba2+ |
|
阴离子 |
Cl-、SO |
现进行以下实验,
①将乙的溶液分别加到足量甲、丁两溶液中时均产生稳定的白色沉淀;
②将少量丙溶液滴入丁溶液时产生白色沉淀,当丙过量时沉淀完全溶解;
③甲、丙两溶液混合时产生的白色沉淀,经分析其中含有两种成份。
据此回答下列问题:
(1)写出下列物质的化学式:甲 乙
(2)丙的阴离子的电子式是 ,丁的阳离子的结构示意图是 ;
(3)写出相应离子方程式:
①甲溶液与丙溶液混合:
②乙溶液与丁溶液混合:
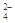 、NO3-、OH-
、NO3-、OH-