题目内容
【题目】综合利用CO2、CO对构建低碳社会有重要意义。
⑴ Li2O、Na2O、MgO均能吸收CO2。如果寻找吸收CO2的其他物质,下列建议合理的是_______。
a.可在碱性氧化物中寻找
b.可在ⅠA、ⅡA族元素形成的氧化物中寻找
c.可在具有强氧化性的物质中寻找
⑵ Li4SiO4可用于吸收、释放CO2,原理是:在500℃,CO2与Li4SiO4接触后生成Li2CO3;平衡后加热至700℃,反应逆向进行,放出CO2,Li4SiO4再生。写出CO2与Li4SiO4反应的化学方程式______________;该反应为_______(填“吸”或者“放”)热反应,原因是_____________________。
⑶ CO与H2在催化剂作用下发生如下反应:CO(g)+2H2(g)![]() CH3OH(g)。对此反应进行如下研究:某温度下在某2 L恒容密闭容器中分别充入1.2 mol CO和 1 mol H2,达到平衡测得有0.4 mol CH3OH(g),则该反应平衡常数值为_____________。
CH3OH(g)。对此反应进行如下研究:某温度下在某2 L恒容密闭容器中分别充入1.2 mol CO和 1 mol H2,达到平衡测得有0.4 mol CH3OH(g),则该反应平衡常数值为_____________。
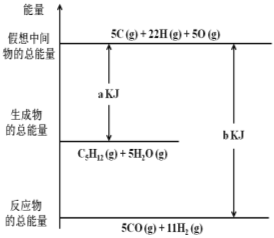
⑷ 在200℃并用钴做催化剂的条件下,CO与H2可合成C5H12(汽油的一种成分),可减少碳排放。反应中能量变化如下图所示,写出该反应的热化学方程式____________。
【答案】(11分)(除标注外,每空2分)
(1)ab(2)2CO2+Li4SiO4![]() 2Li2CO3+SiO2;放(1分),
2Li2CO3+SiO2;放(1分),
升高温度,平衡向逆向进行,说明逆反应为吸热反应,所以正反应为放热反应。
(3)50(4)5CO(g)+11H2(g)![]() C5H12(g)+5H2O(g)H=+(b-a)KJ/mol
C5H12(g)+5H2O(g)H=+(b-a)KJ/mol
【解析】
试题分析:(1)a.Li2O、Na2O、MgO均属于碱性氧化物,均能吸收酸性氧化物CO2,可在碱性氧化物中寻找吸收CO2的其他物质,故a正确;b.Li2O、Na2O、MgO均能吸收CO2,钠、镁为ⅠA、ⅡA族元素,所以可在ⅠA、ⅡA族元素形成的氧化物中寻找吸收CO2的其他物质,故b正确;c.Li2O、Na2O、MgO均能吸收CO2,但它们都没有强氧化性,且吸收二氧化碳与氧化还原无关,故c错误;故答案为ab;
(2)在500℃,CO2与Li4SiO4接触后生成Li2CO3,反应物为CO2与Li4SiO4,生成物有Li2CO3,根据质量守恒可知产物还有Li2SiO3,所以化学方程式为:CO2+Li4SiO4![]() Li2CO3+Li2SiO3;由于升高温度平衡左移,故正反应为放热反应;
Li2CO3+Li2SiO3;由于升高温度平衡左移,故正反应为放热反应;
(3)CO(g)+2H2(g)CH3OH(g)
起始:1.2mol 1mol 0
转化:0.4mol 0.8mol 0.4mol
平衡:0.8mol 0.2mol 0.4mol
所以:k=![]() =50(mol/L)-2;
=50(mol/L)-2;
(4)根据图1可知,反应物为5molCO气体和11mol氢气,产物为1mol戊烷气体和5mol水蒸汽,由于反应物的能量低于产物的能量,故此反应为吸热反应,且吸收(b-a)KJ,故热化学方程式为:5CO(g)+11H2(g)═C5H12(g)+5H2O(g)△H=+(b-a) KJ/mol。

【题目】
(1)化学平衡常数K表示可逆反应进行程度,K值越大,表示 ,K值大小与温度的关系是:△H<0(正反应放热),当温度升高K值 。
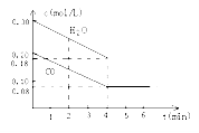
(2)在一体积为10L的容器中,通入一定量的CO和H2O(g),在850℃时发生如下反应:CO(g) + H2O(g)![]() CO2(g)+H2(g) △H<0,CO和H2O浓度变化如下图所示,则0~4min的平均速率v(CO)= 。
CO2(g)+H2(g) △H<0,CO和H2O浓度变化如下图所示,则0~4min的平均速率v(CO)= 。
(3)t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表。
t1℃时物质浓度(mol/L)的变化
时间(min) | CO | H2O | CO2 | H2 |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | c1 | c2 | c3 | c3 |
4 | c1 | c2 | c3 | c3 |
5 | 0.116 | 0.216 | 0.084 | |
6 | 0.096 | 0.266 | 0.104 |
①表中3~4min反应处于 状态;c1数值 0.08mol/L(填“>”“<”“=”)
②反应在4~5min,平衡向逆方向移动,可能的原因是 (单选),表中5~6min数值发生变化,可能的原因是 (单选)
A.增加水蒸气 B.降低温度 C.使用催化剂 D.增加氢气浓度