题目内容
下列除去杂质的实验操作,能达到实验目的是( )
| A、除去FeCl2溶液中少量的FeCl3:加入稍过量Fe粉后过滤 | B、除去K2CO3固体中少量NaHCO3:置于坩埚中加热至质量不再变化 | C、除去HCl气体中少量Cl2:将其依次通过饱和食盐水、无水CaCl2 | D、除去NaNO3溶液中少量Ba(NO3)2:向其中依次滴加过量Na2CO3溶液、适量盐酸 |
分析:A.Fe与FeCl3反应生成FeCl2;
B.NaHCO3受热分解生成碳酸钠,引入新杂质;
C.Cl2极易溶于水,食盐水抑制HCl的溶解,然后干燥即可;
D.Ba(NO3)2与过量Na2CO3溶液反应生成沉淀和硝酸钠,但碳酸钠过量,再加盐酸生成NaCl.
B.NaHCO3受热分解生成碳酸钠,引入新杂质;
C.Cl2极易溶于水,食盐水抑制HCl的溶解,然后干燥即可;
D.Ba(NO3)2与过量Na2CO3溶液反应生成沉淀和硝酸钠,但碳酸钠过量,再加盐酸生成NaCl.
解答:解:A.Fe与FeCl3反应生成FeCl2,然后过滤可实现除杂,故A正确;
B.NaHCO3受热分解生成碳酸钠,引入新杂质,则加热至质量不变不能实现除杂,故B错误;
C.Cl2极易溶于水,食盐水抑制HCl的溶解,然后利用无水CaCl2干燥即可实现除杂,故C正确;
D.Ba(NO3)2与过量Na2CO3溶液反应生成沉淀和硝酸钠,但碳酸钠过量,再加盐酸生成NaCl,引入新杂质,故D错误;
故选AC.
B.NaHCO3受热分解生成碳酸钠,引入新杂质,则加热至质量不变不能实现除杂,故B错误;
C.Cl2极易溶于水,食盐水抑制HCl的溶解,然后利用无水CaCl2干燥即可实现除杂,故C正确;
D.Ba(NO3)2与过量Na2CO3溶液反应生成沉淀和硝酸钠,但碳酸钠过量,再加盐酸生成NaCl,引入新杂质,故D错误;
故选AC.
点评:本题考查混合物分离、提纯方法的选择和应用,为高频考点,把握物质的性质及分离方法为解答的关键,侧重混合物除杂的考查,注意除杂不能引入新杂质,题目难度不大.

练习册系列答案
相关题目
(8分)实验室可用NH4HCO3和NaCl为原料制备纯碱。请根据下表数据和实验步骤,回答下列问题: 30℃时几种盐的溶解度/g
| NaCl | NH4HCO3 | NaHCO3 | NH4Cl | Na2SO4 | (NH4)2SO4 | CaCl2 | MgCl2 | CaSO4 |
| 36.3 | 27.0 | 11.1 | 41.4 | 40.8 | 78 | 51.7 | 26.2 | 0.165 |
①配制50 mL约25%的粗食盐水溶液(密度近似为1 g/mL)。
②精制食盐水(粗食盐中含有少量Ca2+、Mg2+、SO42-等杂质),用盐酸将滤液的pH值调至7。
③加热食盐水,将溶液温度控制在30 ─ 35℃。
④在不断搅拌下,分次将研细的NH4HCO3加入食盐水中,加完料后,继续保温、搅拌半小时。
⑤静置,趁热过滤,回收母液。晶体用蒸馏水洗涤两次。
⑥将晶体灼烧,得到纯碱。
(1)步骤①中,配制溶液的最后一步操作是 ;
(2)步骤②中,SO42-是否需要加入某种试剂除去? ,理由是
(3)步骤④中所有操作的共同目的是 ;
(4)步骤⑤中晶体的洗涤液中主要含有的杂质阳离子是 ,在通常情况下,检验这种阳离子的实验操作为 。
(8分)实验室可用NH4HCO3和NaCl为原料制备纯碱。请根据下表数据和实验步骤,回答下列问题: 30℃时几种盐的溶解度/g
|
NaCl |
NH4HCO3 |
NaHCO3 |
NH4Cl |
Na2SO4 |
(NH4)2SO4 |
CaCl2 |
MgCl2 |
CaSO4 |
|
36.3 |
27.0 |
11.1 |
41.4 |
40.8 |
78 |
51.7 |
26.2 |
0.165 |
制备纯碱的步骤如下:
① 配制50 mL约25%的粗食盐水溶液(密度近似为1 g/mL)。
② 精制食盐水(粗食盐中含有少量Ca2+、Mg2+、SO42-等杂质),用盐酸将滤液的pH值调至7。
③ 加热食盐水,将溶液温度控制在30 ─ 35℃。
④ 在不断搅拌下,分次将研细的NH4HCO3加入食盐水中,加完料后,继续保温、 搅拌半小时。
⑤ 静置,趁热过滤,回收母液。晶体用蒸馏水洗涤两次。
⑥ 将晶体灼烧,得到纯碱。
(1)步骤①中,配制溶液的最后一步操作是 ;
(2)步骤②中,SO42-是否需要加入某种试剂除去? ,理由是
(3)步骤④中所有操作的共同目的是 ;
(4)步骤⑤中晶体的洗涤液中主要含有的杂质阳离子是 ,在通常情况下,检验这种阳离子的实验操作为 。
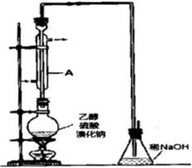 溴乙烷是一种重要的有机化工原料,其沸点为38.4℃.制备溴乙烷的一种方法是乙醇与氢溴酸反应,该反应的化学方程式是
溴乙烷是一种重要的有机化工原料,其沸点为38.4℃.制备溴乙烷的一种方法是乙醇与氢溴酸反应,该反应的化学方程式是
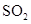 生成,同时观察到还有一种红棕色气体产生,该气体物质的电子式是
。
生成,同时观察到还有一种红棕色气体产生,该气体物质的电子式是
。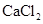 ,然后进行的实验操作是
(填写正确选项的字母)。
,然后进行的实验操作是
(填写正确选项的字母)。 溶液 ③加入稀
溶液 ③加入稀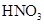 酸化
④加入NaOH溶液
酸化
④加入NaOH溶液