题目内容
在500mLCuSO4溶液中插入两根电极,一极为铁,另一极为含杂质锌均匀的粗铜,通电一段时间后,切断电源,立即将电极取出,这时铁极上析出7.04g铜,电解液增重0.02g。求粗铜中锌的质量分数。
18.4%(6分)
铁极析出铜,发生还原反应,为阴极:Cu2++2e-=Cu
而粗铜为阳极:Zn=2e-=Zn2+ Cu=2e-=Cu2+
铁极质量的增加是由于反应:
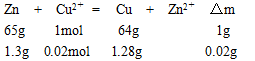
故当阴极有1.3g锌溶解时,同时阴极溶解的铜为7.04-1.28=5.76g
故粗铜中锌的质量分数为 18.4%
18.4%
而粗铜为阳极:Zn=2e-=Zn2+ Cu=2e-=Cu2+
铁极质量的增加是由于反应:
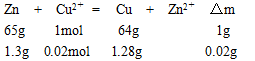
故当阴极有1.3g锌溶解时,同时阴极溶解的铜为7.04-1.28=5.76g
故粗铜中锌的质量分数为
 18.4%
18.4%
练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目