��Ŀ����
����Ŀ����ͼ�ش��������⣺

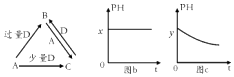
��.�����ձ�����ҺΪϡ���ᣬ��۲쵽�������� ��������ӦʽΪ ��
�����ձ�����ҺΪ����������Һ����Ϊ (�Mg����Al��)���ܷ�Ӧ�Ļ�ѧ����ʽΪ ��
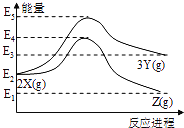
��.�й���ѧԺ����Ӧ�û�ѧ�о����ڼ״�ȼ�ϵ�ؼ�����������ͻ�ƣ���װ�����Ժ�����ؼ�����ʽ��ѡ��״�ȼ�ϵ�صĹ���ԭ����ͼ��ʾ��

���õ�ع���ʱ��b��ͨ�������Ϊ ��c��ͨ�������Ϊ ��
���õ�ظ����ĵ缫��ӦʽΪ ��
������һ��ʱ���12.8 g�״���ȫ��Ӧ����CO2ʱ���� NA������ת�ơ�
���𰸡���16�֣�ÿ��2�֣�
��.��Mg���ܽ⣬AlƬ��������ð����������ָ��ƫת Mg2e![]() Mg2+
Mg2+
��Al 2Al+2NaOH+2H2O![]() 2NaAlO2+3H2��
2NaAlO2+3H2��
��.��CH3OH O2�����
��CH3OH6e+H2O![]() CO2��+6H+
CO2��+6H+
��2.4
����������.�����ձ�����ҺΪϡ���ᣬ��Mg�Ļ����Խ�Alǿ����Mg�������������Ϸ�����ӦMg2e![]() Mg2+��þƬ�ܽ⣻Al�������������Ϸ�����Ӧ2H++2e
Mg2+��þƬ�ܽ⣻Al�������������Ϸ�����Ӧ2H++2e![]() H2������AlƬ��������ð�������·�в����������ʵ�����ָ��ƫת��
H2������AlƬ��������ð�������·�в����������ʵ�����ָ��ƫת��
�����ձ�����ҺΪ����������Һ����ΪMg����NaOH��Һ��Ӧ������Al�Ǹ�����Mg���������ܷ�ӦΪ2Al+2NaOH+2H2O![]() 2NaAlO2+3H2����
2NaAlO2+3H2����
��.��H+�ƶ������֪�����Ϊ�������Ҳ�Ϊ��������b��ͨ��CH3OH��c��ͨ��O2�������������ӦʽΪCH3OH6e+H2O![]() CO2��+6H+����12.8 g�״�(��0.4 mol)��ȫ��Ӧ����CO2ʱ��ת��2.4 mol���ӣ���ת��2.4NA�����ӡ�
CO2��+6H+����12.8 g�״�(��0.4 mol)��ȫ��Ӧ����CO2ʱ��ת��2.4 mol���ӣ���ת��2.4NA�����ӡ�

����Ŀ���о��л���Ľṹ�Ǹ��õ�Ӧ���л����ǰ��
��1��![]() ��
��![]() �����л�����Ի��ܣ����й��������±���
�����л�����Ի��ܣ����й��������±���
����ܶ�/�� | �۵� | �е� | �ܽ��� | |
|
|
|
| ������ˮ |
|
|
|
| ��ˮ������Ȼ��� |
��Ҫ��ȥ![]() ��
��![]() �Ļ�����е�
�Ļ�����е�![]() ��������_________�������ɵõ��ϴ���
��������_________�������ɵõ��ϴ���![]() ��
��
A������ B���ؽᾧ C����ȡ D����ˮ�������Һ
��Ϊ�ⶨ![]() �Ľṹ����������ʵ�飺��һ����
�Ľṹ����������ʵ�飺��һ����![]() �����������г��ȼ�գ�ʵ��������
�����������г��ȼ�գ�ʵ��������![]() ��
�� ![]() ����������6��72 L����״���£��������Dzⶨ���л�����Է�����Ϊ
����������6��72 L����״���£��������Dzⶨ���л�����Է�����Ϊ![]() ������л���ķ���ʽΪ__________��д��
������л���ķ���ʽΪ__________��д��![]() �����п��ܵĽṹ��ʽ____________________________________��
�����п��ܵĽṹ��ʽ____________________________________��
��������ͼ��ʾ![]() ����Է�������Ϊ
����Է�������Ϊ![]() �����������ʾ�жԳ�
�����������ʾ�жԳ�![]() ���Գ�
���Գ�![]() ����
����![]() ����
����![]() �Ľṹ��ʽΪ____________________________________��
�Ľṹ��ʽΪ____________________________________��
��2���ڳ����²ⶨ��Է�������Ϊ![]() ��ij���ĺ˴Ź������ף���Ϊ�������۲쵽�������͵�
��ij���ĺ˴Ź������ף���Ϊ�������۲쵽�������͵�![]() ԭ�Ӹ������źţ���ǿ��֮��Ϊ
ԭ�Ӹ������źţ���ǿ��֮��Ϊ![]() ����������Ľṹ��ʽΪ____________________________________����Ϊ���㣬��һ�ȴ�����
����������Ľṹ��ʽΪ____________________________________����Ϊ���㣬��һ�ȴ�����![]() �֣�������Ľṹ��ʽΪ______________________��
�֣�������Ľṹ��ʽΪ______________________��
��3��ijϩ��![]() ����Է�������Ϊ
����Է�������Ϊ![]() ��
��![]() ��
��![]() �����ӳɷ�Ӧ�õ�������ֻ�������ִ���˳���칹��ϩ��
�����ӳɷ�Ӧ�õ�������ֻ�������ִ���˳���칹��ϩ��![]() �������ӳɵõ������ϩ����˳ʽ�Ľṹ��ʽΪ________������Ϊ________��
�������ӳɵõ������ϩ����˳ʽ�Ľṹ��ʽΪ________������Ϊ________��