题目内容
配制250 mL 0.5 mol·L-1的NaOH溶液,在下列仪器中:①量筒 ②250 mL容量瓶 ③托盘天平和砝码 ④500 mL容量瓶 ⑤烧杯 ⑥玻璃棒 ⑦漏斗 ⑧药匙 ⑨胶头滴管
⑩250 mL的烧瓶,需要用到的仪器按使用先后顺序排列正确的是
⑩250 mL的烧瓶,需要用到的仪器按使用先后顺序排列正确的是
| A.⑧③⑤⑥②⑨ | B.②③⑦⑤⑥ |
| C.②⑤⑦⑥① | D.④③⑦⑤⑥ |
A
试题分析:本题只需一步即可选出答案,在用固体配置溶液时,首先要用药匙取所需药品,然后用托盘天平称量,用烧杯、玻璃棒溶解,再选择一定规格的容量瓶,最后用胶头滴管定容,而选项中只有A符合,因此答案选A。B、C、D均错。

练习册系列答案
相关题目
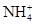 的物质的量为b mol。下列叙述中正确的是( )
的物质的量为b mol。下列叙述中正确的是( )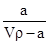 ×100%
×100%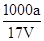 mol/L
mol/L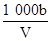 mol/L
mol/L