题目内容
【题目】某化学兴趣小组的同学在分析甲酸的组成和结构后,对甲酸的性质提出如下猜想并设计了相关实验加以验证: 猜想Ⅰ:甲酸具有酸性
实验Ⅰ:在甲酸溶液中滴加紫色石蕊试液
猜想Ⅱ:甲酸能发生酯化反应
实验Ⅱ:[装置如图(1)所示]
猜想Ⅲ:甲酸能发生银镜反应
实验Ⅲ:[步骤如图(2)所示]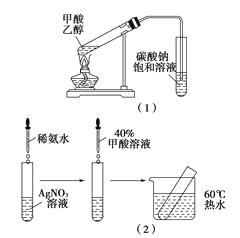
(1)问题Ⅰ:请你进一步设计实验证明甲酸是强酸还是弱酸?
(2)问题Ⅱ:实验Ⅱ能验证猜想Ⅱ吗?;如能,请说明你的理由;如不能,请指出实验Ⅱ中的错误。
(3)问题Ⅲ:分析甲酸的结构,实验Ⅲ中没有出现任何现象的可能原因是。
(4)问题Ⅳ:请你在仔细分析甲酸的组成和结构的基础上,再提出一个关于甲酸性质的猜想并设计实验方案验证你的猜想: ①你提出的猜想是。
②你设计的实验方案是。
【答案】
(1)测定HCOONa溶液的pH(或将等pH的HCOOH溶液和HCl溶液稀释相同倍数测其pH的变化或比较等浓度甲酸和盐酸的导电性等)
(2)不能;反应混合液中没有浓硫酸;吸收装置中导管伸到饱和碳酸钠溶液液面以下
(3)由于羟基对醛基的影响,导致甲酸中的醛基不具有典型醛基的性质
(4)甲酸在浓硫酸的作用下脱水生成CO和H2O;浓硫酸加热 氧化铜加热
【解析】问题Ⅰ的证明方法很多,相当于验证HCOOH是强电解质还是弱电解质。图(1)是酯化反应的实验,很显然有两个不当之处,一是没有使用催化剂浓硫酸致使酯化反应很难发生,二是导管不能插入饱和碳酸钠溶液的下方,易引起倒吸。不能盲目回答问题Ⅲ,从图(2)的实验操作过程上分析应该没有问题,题目提示要从甲酸结构上分析,甲酸可看成醛基连接一个羟基;因此实验Ⅲ中没有出现任何现象的可能原因是羟基的影响。

练习册系列答案
相关题目