题目内容
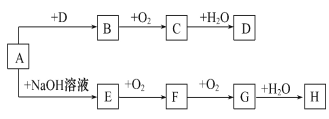
【题目】A~H8种物质存在如下转化关系(反应条件,部分产物未标出)。已知:A是酸式盐,B是能使品红溶液褪色的气体,G是红棕色气体。按要求回答问题:
(1)写出下列物质的化学式:A___________。
(2)写出下列反应的化学方程式:
B与E按1:2通入水中_________;
G→H_______
D的浓溶液与红热的木炭反应的方程式:______
(3)检验某溶液中是否含D中阴离子的方法:__________________。
【答案】NH4HSO3 2NH3+SO2+H2O =(NH4)2SO3 3NO2+H2O====2HNO3+NO C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O 取少量被检验溶液注入一支试管中,然后向试管中滴加盐酸,溶液无明显现象,然后滴加BaCl2溶液,若产生白色沉淀,说明溶液中存在SO42-,否则溶液中不存在SO42-
CO2↑+2SO2↑+2H2O 取少量被检验溶液注入一支试管中,然后向试管中滴加盐酸,溶液无明显现象,然后滴加BaCl2溶液,若产生白色沉淀,说明溶液中存在SO42-,否则溶液中不存在SO42-
【解析】
G是红棕色气体,则G是NO2,F和氧气反应生成二氧化氮,所以F是NO,二氧化氮和水反应生成H是HNO3.A是酸式盐,和氢氧化钠反应生成E,E和氧气反应生成NO,则E是NH3,B能使品红溶液褪色,且B能和氧气反应生成C,所以B是SO2,C是SO3,三氧化硫和水反应生成D为H2SO4,A是酸式盐且是铵盐,所以A是NH4HSO3,据此答题。
由分析可知:A是NH4HSO3,B是SO2,C是SO3,D为H2SO4,E是NH3,F是NO,G是NO2,H是HNO3。
(1)通过以上分析可知,A是NH4HSO3,故答案为:NH4HSO3。
(2)SO2与NH3按1:2通入水中反应生成亚硫酸铵,反应方程式为2NH3+SO2+H2O=(NH4)2SO3;G→H为二氧化氮与水反应生成硝酸与一氧化氮,反应方程式为3NO2+H2O=2HNO3+NO;木炭和浓硫酸在加热条件下反应生成二氧化硫、二氧化碳和水,反应方程式为C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O;故答案为:2NH3+SO2+H2O=(NH4)2SO3;3NO2+H2O=2HNO3+NO;C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O;故答案为:2NH3+SO2+H2O=(NH4)2SO3;3NO2+H2O=2HNO3+NO;C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。
(3)D为H2SO4,其阴离子为SO42-,SO42-的检验方法为:取少量被检验溶液注入一支试管中,然后向试管中滴加盐酸,溶液无明显现象,然后滴加BaCl2溶液,若产生白色沉淀,说明溶液中存在SO42-,否则溶液中不存在SO42-,故答案为:取少量被检验溶液注入一支试管中,然后向试管中滴加盐酸,溶液无明显现象,然后滴加BaCl2溶液,若产生白色沉淀,说明溶液中存在SO42-,否则溶液中不存在SO42-。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案