题目内容
下列关于氧化还原反应说法正确的是
| A.肯定有一种元素被氧化,另外一种或多种元素被还原 |
| B.某元素从化合态变成游离态,该元素一定被还原 |
| C.氧化还原反应的本质是元素的化合价发生改变 |
| D.在反应中不一定所有元素的化合价都发生变化 |
D
解析试题分析:A选项有可能在反应中只有一个元素发生价态变化,错误。B选项元素从化合态变成游离态,可能被氧化,也可能被还原,错误。C选项氧化还原的本质是电子的转移,错误。D选项正确。
考点:氧化还原的基本概念

下列反应类型的判断,不正确的是( )
A.CO2+H2O H2CO3化合反应 H2CO3化合反应 |
B.Cu(OH)2 CuO+H2O 分解反应 CuO+H2O 分解反应 |
C.MnO2+2CO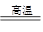 Mn+2CO2置换反应 Mn+2CO2置换反应 |
| D.NaCl+AgNO3=AgCl↓+NaNO3复分解反应 |
发射“嫦娥二号”的长征火箭由三个子级构成。其中一子级上部装有液体四氧化二氮(N2O4),下部装有液体偏二甲肼(C2H8N2)高能燃料。发动机内燃烧的化学方程式为:C2H8N2+2N2O4=3N2↑+2CO2↑+4H2O↑,该反应中
| A.C2H8N2发生还原反应 | B.C2H8N2是氧化剂 |
| C.N2O4发生氧化反应 | D.N2O4是氧化剂 |
为使Fe2+,Fe3+,Zn2+较完全地形成氢氧化物沉淀,溶液的酸碱度分别为pH7.7、 pH4.5、pH6.6。某硫酸锌酸性溶液中含有少量Fe2+,Fe3+杂质离子,为除去这些离子制得纯净的ZnSO4,应加入的试剂是
| A.H2O2,ZnO | B.氨水 | C.KMnO4,ZnCO3 | D.NaOH溶液 |
工业废气中氮氧化物是造成污染的主要来源之一.为了防治污染,工业上常通入氨气与氮氧化物反应:NOx+NH3→N2+H2O.现有NO、NO2的混合气体3L,可用同温同压下的NH3 3.5L恰好与它完全反应生成N2。则原混合气体中NO和NO2的物质的量之比为( )
| A.1∶1 | B.1∶3 | C.2∶1 | D.1∶4 |
对于反应:2H2S+SO2="3S" +2H2O,被氧化的硫原子与被还原的硫原子的质量之比为( )
| A.1:1 | B.2:1 | C.3:1 | D.1:2 |
今有下列三个氧化还原反应:①2FeCl3+2KI 2KCl+2FeCl2+I2
2KCl+2FeCl2+I2
②2Fe+3Cl2 2FeCl3 ③2KMnO4+16HCl
2FeCl3 ③2KMnO4+16HCl 2KCl+2MnCl2+5Cl2↑+8H2O,若某溶液中有Fe2+、I-和Cl-共存,要氧化除去I-而不影响Fe2+和Cl-,可加入的试剂是
2KCl+2MnCl2+5Cl2↑+8H2O,若某溶液中有Fe2+、I-和Cl-共存,要氧化除去I-而不影响Fe2+和Cl-,可加入的试剂是
| A.KMnO4 | B.FeCl3 | C.Cl2 | D.HCl |
有关下列三个化学反应的叙述,氧化产物和还原产物物质的量之比为2:1的是
①2H2S+SO2=3S+2H2O ②S+2H2SO4(浓)=3SO2↑+ 2H2O
③3S+6KOH= 2K2S+K2SO3+3H2O
| A.① | B.①② | C.②③ | D.①②③ |
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3→K2O+5Na2O+16N2↑。则下列判断不正确的是
| A.若氧化产物比还原产物多0.35mol,有0.050molKNO3被氧化 |
| B.若氧化产物比还原产物多0.35mol,生成8.96LN2(标准状况) |
| C.若有0.2mol氧化剂反应,则转移电子的物质的量为1.0mol |
| D.KNO3的氧化性强于N2 |