题目内容
8.在硫酸铁溶液中,加入a g铜完全溶解后再加入b g铁,充分反应后得到c g残余固体,下列说法中正确的有( )
①若a>c,则残余固体是铁和Cu的混合物
②若a>c,则最终溶液中一定有Fe2+、和Cu2+
③若a>c,则最终溶液中一定没有Fe3+
④若a<c,则最终溶液中可能有Cu2+
⑤若a<c,则最终溶液中一定有Fe2+.
| A. | 0项 | B. | 1项 | C. | 2项 | D. | 3项 |
分析 在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,向盛有FeCl3溶液的烧杯内分别加入铁粉和铜粉,铁能与氯化铁反应生成氯化亚铁,铜能与氯化铁反应生成氯化亚铁和铜,利用此知识解决即可.
解答 解:此题中发生的化学反应有三个,方程式如下:2FeCl3+Cu=2FeCl2+CuCl2;CuCl2+Fe=FeCl2+Cu;2FeCl3+Fe=3FeCl2
依元素守恒可知
步骤一:ag铜完全溶解后,变为ag铜离子,
步骤二:若加入的铁足够多的话,可将溶液中的铜离子全部变回金属铜(ag)甚至还会有铁剩余,此时,残余固体(cg)应大于或等于ag,
依题意:a>c可知,加入的铁是不足量的,此时溶液中还有部分铜未完全置换出来.
结论1:剩余固体为Cu,不可能有Fe剩,溶液中不可能存在Fe3+离子,故①错误、③正确,
步骤三:根据方程式可知,溶液中一定有Fe2+,因上述推导可知,溶液中还应有Cu2+剩余,由方程式1可知,Cu与Fe3+是不能共存的,剩余固体中有Cu,则溶液中必无Fe3+
结论2:充分反应后剩余固体为Cu,而溶液中含FeCl2和CuCl2,②正确;
当a<c可知,cg中含有铜,同时铁过量,溶液中不可能含铜离子,铁离子被还原为亚铁离子,最终溶液中一定有Fe2+.故④错误、⑤正确;
所以有三组正确,
故选D
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行,要注意根据铁和铜的活动性强弱确定反应的先后顺序,题目难度中等.

练习册系列答案
相关题目
18.食用菜油混有了自来水,你将选择下列何种最简便的方法分离它们( )
| A. | 过滤 | B. | 蒸馏 | C. | 分液 | D. | 萃取 |
19.下列说法中错误的是( )
| A. | AgBr见光会分解,可用于制感光材料 | |
| B. | 碳酸氢钠受热会分解,可用作糕点发酵粉 | |
| C. | 因氯气有毒,不能用于对自来水消毒杀菌 | |
| D. | 由于钝化,浓硫酸可用铝槽车运输 |
16.下列仪器能用来直接加热的是( )
| A. | 烧杯 | B. | 蒸发皿 | C. | 烧瓶 | D. | 锥形瓶 |
3.关于Na2CO3和NaHCO3性质的有关叙述正确的是( )
| A. | 在水中溶解性:Na2CO3<NaHCO3 | |
| B. | 热稳定性:Na2CO3<NaHCO3 | |
| C. | 相同条件下与酸反应的快慢Na2CO3<NaHCO3 | |
| D. | Na2CO3不能转化成NaHCO3,而NaHCO3能转化为Na2CO3 |
13.下列离子方程式书写正确的是( )
| A. | AlCl3溶液中加入过量氨水Al3++4NH3•H2O═AlO2ˉ+4NH4++2H2O | |
| B. | Ba(OH)2溶液中加入稀硫酸 Ba2++OHˉ+H++SO42-═BaSO4↓+H2O | |
| C. | Cu(OH)2浊液中滴加盐酸 Cu(OH)2+2H+═Cu2++2H2O | |
| D. | NaHCO3溶液与硫酸溶液的反应 HCO3-+H+═H2O+CO2↑ |
18.某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的离子组是( )
| A. | K+ Na+ HCO3- NO3- | B. | Na+ SO42- Cl- ClO- | ||
| C. | H+ Mg2+ SO42- NO3- | D. | Ag+ K+ NO3- Na+ |
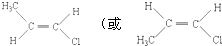 ,另一种名称是反-1-氯丙烯(顺-1-氯丙烯).
,另一种名称是反-1-氯丙烯(顺-1-氯丙烯).