题目内容
【题目】在2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O反应中:
(1)氧化剂是(填化学式) , 还原剂是(填化学式) .
(2)在该反应中,若消耗了15.8g KMnO4 , 则转移了mol 电子.
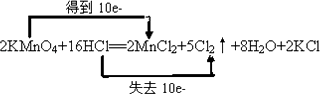
(3)用双线桥表示高锰酸钾和浓盐酸反应的电子转移方向和数目.
2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O.
【答案】
(1)KMnO4,HCl
(2)0.5
(3)
【解析】解:(1)2KMnO4+16HCl═2MnCl2+5Cl2↑+8H2O+2KCl中,Mn元素的化合价降低,KMnO4为氧化剂,Cl元素的化合价升高,HCl为还原剂;
(2)根据Mn元素化合价由+7降低到+2,所以若消耗了15.8g KMnO4,则转移了 ![]() ×(7﹣2)=0.5mol;
×(7﹣2)=0.5mol;
(3)2KMnO4+16HCl═2MnCl2+5Cl2↑+8H2O+2KCl中,Mn元素的化合价降低,KMnO4为氧化剂,Cl元素的化合价升高,HCl为还原剂,该反应转移10e﹣,双线桥标出电子的转移方向和数目为  ;
;
所以答案是:(1)KMnO4;HCl;(2)0.5;(3)

练习册系列答案
相关题目
【题目】如图所示实验中,把四根洁净的金属条A、B、C、D轮流放置在浸有盐溶液的滤纸上面并压紧.在每次轮流实验时,记录了电压表指针的移动方向和电压表的读数(如下表).下列说法中正确的是( )
金属 | 电子流动方向 | 电压 |
A | A→Cu | +0.78 |
B | Cu→B | ﹣2.15 |
C | C→Cu | +1.35 |
D | +0.30 |
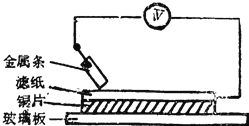
A.金属D与Cu之间电子流动方向为Cu→D
B.A金属可能是最强的还原剂
C.B金属不能从硫酸铜溶液中置换铜
D.B金属可能是最强的还原剂