题目内容
下列表述中正确的是
| A.任何能使熵值增大的过程都能自发进行 |
| B.△H<0,△S>0的化学反应一定能自发进行 |
C.已知热化学方程式2SO2(g)+O2(g) 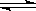 2SO3(g)△H=-QkJ·mol-1(Q>0),则将2mol SO2(g) 和1mol O2(g) 置于一密闭容器中充分反应后放出Q kJ的热量 2SO3(g)△H=-QkJ·mol-1(Q>0),则将2mol SO2(g) 和1mol O2(g) 置于一密闭容器中充分反应后放出Q kJ的热量 |
| D.稀溶液中1mol NaOH分别和1mol CH3COOH、1molHNO3反应,两者放出的热量一样多 |
B
解析试题分析:A、反应能否自发进行不单取决于熵的变化,还受反应热的影响,△G=△H-T·△S,错误;B、从△G=△H-T·△S 中可以看出,△H<0,△S>0的化学反应中,△G<0,一定能自发进行,正确;C、△H=-QkJ·mol-1Q的具体含义是:当2mol 的二氧化硫与1mol 的氧气完全反应生成2mol 的三氧化硫时,放出的热量为QkJ ,但这是一个可逆反应,不可能完全反应,因此放出的热量小于Q kJ,错误;D、1mol NaOH分别和1mol CH3COOH反应时,放出的热量其中有一小部分用于醋酸的电离,因此放出的热量总体上来说就比硝酸与氢氧化钠的反应少一点,错误。
考点:考查反应热以及反应进行的方向的判断。

 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案某兴趣小组经实验测定,在1×105 Pa,298 K条件下,1 mol氢气完全燃烧生成水蒸气放出242 kJ热量,下列热化学方程式正确的是 ( )
A.H2O(g)=H2(g)+ O2(g) ΔH=+242 kJ·mol-1 O2(g) ΔH=+242 kJ·mol-1 |
| B.2H2(g)+O2(g)=2H2O(l) ΔH=-484 kJ·mol-1 |
C.H2(g)+ O2(g)=H2O(g) ΔH=+242 kJ·mol-1 O2(g)=H2O(g) ΔH=+242 kJ·mol-1 |
| D.2H2(g)+O2(g)=2H2O(g) ΔH=+484 kJ·mol-1 |
下列说法正确的是 ( )。
| A.任何化学反应都伴随着能量的变化 |
| B.H2O(g)―→H2O(l)该过程放出大量的热,所以该过程是化学变化 |
| C.化学反应中能量的变化都表现为热量的变化 |
| D.对于如图所示的过程,是吸收能量的过程 |

下列有关热化学方程式或反应热的说法正确的是( )
A.已知:H2(g)+ O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1,则H2的燃烧热为-241.8 kJ·mol-1 O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1,则H2的燃烧热为-241.8 kJ·mol-1 |
| B.已知:S(g)+O2(g)=SO2(g) ΔH1=-Q1;S(s)+O2(g)=SO2(g) ΔH2=-Q2(Q1、Q2均正值),则Q1<Q2 |
C.已知: H2SO4(浓)+NaOH(aq)= H2SO4(浓)+NaOH(aq)= Na2SO4(aq)+H2O(l) ΔH1;CH3COOH(aq)+NH3·H2O(aq)=CH3COONH4(aq)+H2O(l) ΔH2,则有|ΔH1|<|ΔH2| Na2SO4(aq)+H2O(l) ΔH1;CH3COOH(aq)+NH3·H2O(aq)=CH3COONH4(aq)+H2O(l) ΔH2,则有|ΔH1|<|ΔH2| |
D.已知:Fe2O3(s)+3C(石墨,s)=2Fe(s)+3CO(g) ΔH=+489.0 kJ·mol-1;CO(g)+ O2(g)=CO2(g)ΔH=-283.0 kJ·mol-1;C(石墨,s)+O2(g)=CO2(g)ΔH=-393.5 kJ·mol-1,则4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1641 kJ·mol-1 O2(g)=CO2(g)ΔH=-283.0 kJ·mol-1;C(石墨,s)+O2(g)=CO2(g)ΔH=-393.5 kJ·mol-1,则4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1641 kJ·mol-1 |
根据碘与氢气反应的热化学方程式
(ⅰ)I2(g)+H2(g)  2HI(g) ΔH=-9.48 kJ·mol-1
2HI(g) ΔH=-9.48 kJ·mol-1
(ⅱ)I2(s)+H2(g)  2HI(g) ΔH=+26.48 kJ·mol-1
2HI(g) ΔH=+26.48 kJ·mol-1
下列判断正确的是( )
| A.1 mol I2(s)中通入2 g H2(g),反应吸热26.48 kJ |
| B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ |
| C.反应(ⅱ)的反应物总能量比反应(ⅰ)的反应物总能量低 |
| D.反应(ⅰ)放出的热量多,所以产物的能量低,比反应(ⅱ)的产物更稳定 |
下列表述中正确的是( )
A.已知2H2(g)+O2(g) 2H2O(g) ΔH="-483.6" kJ/mol,则氢气的燃烧热为241.8 kJ 2H2O(g) ΔH="-483.6" kJ/mol,则氢气的燃烧热为241.8 kJ |
B.由C(石墨,s) C(金刚石,s) ΔH="+11.9" kJ·mol-1可知,金刚石比石墨稳定 C(金刚石,s) ΔH="+11.9" kJ·mol-1可知,金刚石比石墨稳定 |
C.同温同压下,H2(g)+Cl2(g) 2HCl(g)在光照和点燃条件的ΔH不同 2HCl(g)在光照和点燃条件的ΔH不同 |
| D.任何一个化学变化都伴随着能量的变化 |
某一化学反应在不同条件下的能量变化曲线如下图所示。下列说法正确的是( )
| A.化学催化比酶催化的效果好 |
| B.使用不同催化剂可以改变反应的热效应 |
| C.使用不同催化剂可以改变反应的能耗 |
| D.反应物的总能量低于生成物的总能量 |
已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)ΔH=+489.0 kJ·mol-1①
CO(g)+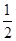 O2(g)=CO2(g)ΔH=-283.0 kJ·mol-1②
O2(g)=CO2(g)ΔH=-283.0 kJ·mol-1②
C(石墨)+O2(g)=CO2(g)ΔH=-393.5 kJ·mol-1③
则4Fe(s)+3O2(g)=2Fe2O3(s)的ΔH为( )
| A.+1 164.1 kJ·mol-1 | B.-1 641.0 kJ·mol-1 |
| C.-259.7 kJ·mol-1 | D.-519.4 kJ·mol-1 |
下图是N2与H2反应生成NH3的过程中能量变化的曲线图:
下列叙述正确的是( )。
| A.该反应的热化学方程式为N2(g)+3H2(g)=2NH3(g) ΔH=-92 kJ |
| B.b曲线是加入催化剂时的能量变化曲线 |
| C.加入催化剂,该化学反应的反应热减小 |
| D.在温度、体积一定的条件下,通入1 mol N2和3 mol H2反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184>Q2>2Q1 |