题目内容
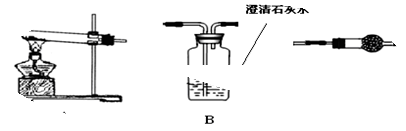
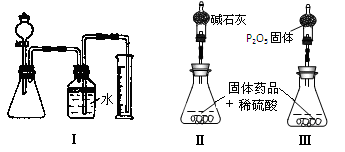
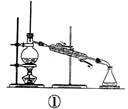
三草酸合铁(Ⅲ)酸钾晶体(K3[Fe(C2O4)3]·3H2O)有很重要的用途。可用如下流程来制备。根据题意完成下列各题:
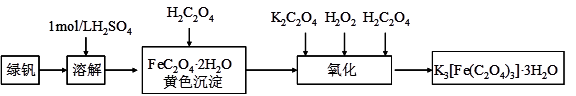
(1)要从溶液中得到绿矾,必须进行的实验操作是 。(按前后顺序填)
a.过滤洗涤 b.蒸发浓缩 c.冷却结晶 d.灼烧 e.干燥
某兴趣小组为测定三草酸合铁酸钾晶体(K3[Fe(C2O4)3]·3H2O)中铁元素含量,做了如下实验:
步骤1:称量5.000g三草酸合铁酸钾晶体,配制成250ml溶液。
步骤2:取所配溶液25.00ml于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部被氧化成二氧化碳,同时,MnO4— 被还原成Mn2+。向反应后的溶液中加入一定量锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍里酸性。
步骤3:在酸性条件下,用0.010mol/L KMnO4溶液滴定步骤二所得溶液至终点,共做三次实验,平均消耗KMnO4溶液20.00ml,滴定中MnO4—,被还原成Mn2+。
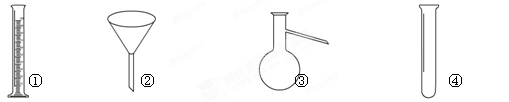
(2)步骤1中,配制三草酸合铁酸钾溶液需要使用的玻璃仪器除烧杯、玻璃棒以外还有 ;
主要操作步骤依次是:称量、溶解、转移、 、定容、摇匀。
(3)步骤2中,加入锌粉的目的是 。
(4)步骤3中,发生反应的离子方程式为: 。
(5)步骤2中,若加入的KMnO4的溶液的量不够,则测得的铁含量 。(选填“偏低”、“偏高”、“不变”)
(6)某同学将8.74 g无水三草酸合铁酸钾(K3[Fe(C2O4)3])在一定条件下加热分解,所得固体的质量为5.42g,同时得到密度为1.647 g/L(已折合成标准状况下)气体(是物质的量之比为4:5的混合气体)。研究固体产物得知,铁元素不可能以三价形式存在,而盐只有K2CO3。写出该分解反应的化学方程式 。

(1)要从溶液中得到绿矾,必须进行的实验操作是 。(按前后顺序填)
a.过滤洗涤 b.蒸发浓缩 c.冷却结晶 d.灼烧 e.干燥
某兴趣小组为测定三草酸合铁酸钾晶体(K3[Fe(C2O4)3]·3H2O)中铁元素含量,做了如下实验:
步骤1:称量5.000g三草酸合铁酸钾晶体,配制成250ml溶液。
步骤2:取所配溶液25.00ml于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部被氧化成二氧化碳,同时,MnO4— 被还原成Mn2+。向反应后的溶液中加入一定量锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍里酸性。
步骤3:在酸性条件下,用0.010mol/L KMnO4溶液滴定步骤二所得溶液至终点,共做三次实验,平均消耗KMnO4溶液20.00ml,滴定中MnO4—,被还原成Mn2+。
(2)步骤1中,配制三草酸合铁酸钾溶液需要使用的玻璃仪器除烧杯、玻璃棒以外还有 ;
主要操作步骤依次是:称量、溶解、转移、 、定容、摇匀。
(3)步骤2中,加入锌粉的目的是 。
(4)步骤3中,发生反应的离子方程式为: 。
(5)步骤2中,若加入的KMnO4的溶液的量不够,则测得的铁含量 。(选填“偏低”、“偏高”、“不变”)
(6)某同学将8.74 g无水三草酸合铁酸钾(K3[Fe(C2O4)3])在一定条件下加热分解,所得固体的质量为5.42g,同时得到密度为1.647 g/L(已折合成标准状况下)气体(是物质的量之比为4:5的混合气体)。研究固体产物得知,铁元素不可能以三价形式存在,而盐只有K2CO3。写出该分解反应的化学方程式 。
(1)bcae (2)250ml容量瓶 洗涤 (3)还原Fe3+为Fe2+
(4)MnO4—+5Fe2++8H+=Mn2++ 5Fe3++4H2O
(5)偏高 (6)2K3[Fe(C2O4)3 3K2CO3+Fe+FeO+4CO+5CO2↑
3K2CO3+Fe+FeO+4CO+5CO2↑
(4)MnO4—+5Fe2++8H+=Mn2++ 5Fe3++4H2O
(5)偏高 (6)2K3[Fe(C2O4)3
 3K2CO3+Fe+FeO+4CO+5CO2↑
3K2CO3+Fe+FeO+4CO+5CO2↑试题分析:(1)FeSO4在水中的溶解度比较大,而且受温度的影响变化较大,所以要从溶液中得到绿矾,必须进行的实验操作是蒸发浓缩、冷却结晶、过滤洗涤、干燥 。选项为b. c. a .e. (2) 配制成250ml无水三草酸合铁酸钾溶液要用250ml容量瓶,主要操作步骤依次是:称量、溶解、转移、洗涤、定容、摇匀。(3)Fe2+不稳定,容易被空气中的氧气氧化为Fe3+。为防止Fe3+的生成,在步骤2中,加入锌粉。(4) KMnO4与Fe2+发生氧化还原反应的离子方程式是:MnO4—+5Fe2++8H+=Mn2++ 5Fe3++4H2O。(5)步骤2中,若加入的KMnO4的溶液的量不够,三草酸合铁酸钾晶体中的草酸根离子偏少,则Fe2+的含量就偏高。即测得的铁含量偏高。(6) 根据无水三草酸合铁酸钾(K3[Fe(C2O4)3])的质量8.74 g可计算其物质的量n(K3[Fe(C2O4)3])=" 8.74" g÷437g/mol=0.02mol,n(K2CO3)=" (0.02mol×3)" ÷2=0.03mol.m(K2CO3)=" 0.03mol×138g/mol=4.14g.n(Fe)=" n(K3[Fe(C2O4)3])=0.02mol。由于在所得固体中无Fe3+。所以Fe只能以Fe单质及FeO的形式存在,假设Fe 、FeO的物质的量分别为M、N。则n(Fe)+n(FeO)=0.02;56M+72N=5.424.14.解得M= 0.01,N=0.01。m(气体)=" 8.74" g-5.42g=3.32g,混合气体的平均摩尔质量为:1.647 g/L×22.4L/mol=36.89g/mol.n(气体)=" 3.32g" ÷36.89g/mol=0.09mol.根据物质的组成元素可知:气体只可能是CO、CO2的混合物。假设CO、CO2的物质的量分别为X、Y。则(28X+44Y)÷(X+Y)=36.89,解得X:Y=4:5。所以n(CO)=0.04mol;n(CO2)=0.05mol.故 n(K3[Fe(C2O4)3]): n(K2CO3): n(Fe): n(FeO): n(CO): n(CO2)=0.02:0.03:0.01:0.01:0.04:0.05=2:3:1:1:4: 5.所以Fe(C2O4)3]分解的化学方程式为:K3[Fe(C2O4)3]
 3K2CO3+Fe+FeO+4CO+5CO2↑
3K2CO3+Fe+FeO+4CO+5CO2↑
练习册系列答案
相关题目