题目内容
(2009?肇庆二模)氟化钠是一种重要的氟盐,主要用作农业杀菌剂、杀虫剂、木材防腐剂和生产含氟牙膏等.实验室可通过下图所示的流程以氟硅酸(H2SiF6)等物质为原料制取氟化钠,并得到副产品氯化铵:
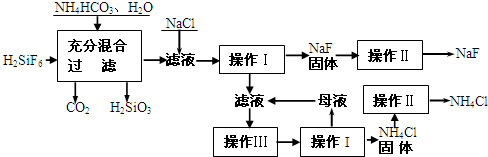
有关物质在水中溶解度见下表.请回答下列问题:
(1)操作Ⅰ需要用到的玻璃仪器有玻璃棒、烧杯、
(2)上述流程中发生两步化学反应,第一步反应的化学方程式为:
(3)操作II的作用是
(4)流程中NH4HCO3必须过量,其原因是
(5)NaF可用于生产含氟牙膏,使用含氟牙膏可以预防龋齿.请说明含有NaF的牙膏如何将羟基磷酸钙[Ca5(PO4)3(OH)]转化为更难溶的氟磷酸钙[Ca5(PO4)3F]

有关物质在水中溶解度见下表.请回答下列问题:
| 温度 | 10℃ | 20℃ | 30℃ | 溶解度:20℃NaF-4g;0℃NH4F-100g; 常温Na2SiF6-微溶于水 |
| NH4Cl溶解度 | 33.3g | 37.2g | 41.4g |
漏斗
漏斗
.(2)上述流程中发生两步化学反应,第一步反应的化学方程式为:
H2SiF6+6NH4HCO3=6NH4F+H2SiO3↓+6CO2↑+3H2O
H2SiF6+6NH4HCO3=6NH4F+H2SiO3↓+6CO2↑+3H2O
,第二步反应的化学方程式为NH4F+NaCl=NH4Cl+NaF↓
NH4F+NaCl=NH4Cl+NaF↓
.(3)操作II的作用是
除去NaF、NH4Cl表面的杂质
除去NaF、NH4Cl表面的杂质
;操作Ⅲ的具体过程是蒸发浓缩溶液,析出多量固体后冷却
蒸发浓缩溶液,析出多量固体后冷却
.(4)流程中NH4HCO3必须过量,其原因是
保证H2SiF6能全部反应;防止在加入NaCl后H2SiF6与NaCl反应生成Na2SiF6沉淀混入NaF中影响NaF纯度
保证H2SiF6能全部反应;防止在加入NaCl后H2SiF6与NaCl反应生成Na2SiF6沉淀混入NaF中影响NaF纯度
.(5)NaF可用于生产含氟牙膏,使用含氟牙膏可以预防龋齿.请说明含有NaF的牙膏如何将羟基磷酸钙[Ca5(PO4)3(OH)]转化为更难溶的氟磷酸钙[Ca5(PO4)3F]
羟基磷酸钙在水中存在溶解平衡:Ca5(PO4)3(OH)?5Ca2++3PO43-+OH-,当F-与Ca2+、PO43-结合生成了更难溶于水的Ca5(PO4)3F,使上述平衡中Ca2+和PO43-减少而向右移动,继续生成更多的Ca5(PO4)3F,难溶物发生了转化
羟基磷酸钙在水中存在溶解平衡:Ca5(PO4)3(OH)?5Ca2++3PO43-+OH-,当F-与Ca2+、PO43-结合生成了更难溶于水的Ca5(PO4)3F,使上述平衡中Ca2+和PO43-减少而向右移动,继续生成更多的Ca5(PO4)3F,难溶物发生了转化
.分析:本题主要考查了化学与工业生产的相关知识.第一步反应的方程式,根据已知反应物和生成物,可推知其余生成物,配平即得反应方程式.第二步反应是将第一步生成的NH4F转化为NaF,加入的反应物为NaCl,利用了物质在溶液中溶解度越小则优先析出的特性,所以NaF比NaCl的溶解性小.操作Ⅰ是过滤操作,用到的玻璃仪器包括烧杯、玻璃棒、漏斗;操作Ⅱ是将粗NaF洗涤除去其表面的杂质.操作Ⅲ是将滤液中的溶质进一步提取,故操作是加热蒸发溶剂,析出大量固体后冷却;流程中NH4HCO3必须过量,是指第一步操作中必须保证H2SiF6能全部反应,以防止生成影响制取物质的纯度.
解答:解:(1)操作Ⅰ是过滤操作,用到的玻璃仪器包括烧杯、玻璃棒、漏斗,故答案为:漏斗;
(2)第一步反应的方程式,反应物有H2SiF6、和NH4HCO3,生成物有H2SiO3、CO2,根据质量守恒还应有NH4F,则反应的化学方程式为H2SiF6+6NH4HCO3=6NH4F+H2SiO3↓+6CO2↑+3H2O,第二步反应是将第一步生成的NH4F转化为NaF,加入的反应物为NaCl,利用了物质在溶液中溶解度越小则优先析出的特性,所以NaF比NaCl的溶解性小,反应的化学方程式为
NH4F+NaCl=NH4Cl+NaF↓,
故答案为:H2SiF6+6NH4HCO3=6NH4F+H2SiO3↓+6CO2↑+3H2O;NH4F+NaCl=NH4Cl+NaF↓;
(3)操作Ⅱ是将粗NaF洗涤除去其表面的杂质,以得到纯净的NaF,操作Ⅲ是将滤液中的溶质进一步提取,故操作是加热蒸发溶剂,析出大量固体后冷却,
故答案为:除去NaF、NH4Cl 表面的杂质;蒸发浓缩溶液,析出多量固体后冷却;
(4))流程中NH4HCO3必须过量,是指第一步操作中必须保证H2SiF6能全部反应,以防止生成Na2SiF6沉淀,影响制取物质的纯度,
故答案为:保证H2SiF6能全部反应;防止在加入NaCl后H2SiF6与NaCl反应生成Na2SiF6沉淀混入NaF中影响NaF纯度;
(5)从沉淀平衡移动的角度分析,Ca5(PO4)3F的溶解度小于Ca5(PO4)3(OH),羟基磷酸钙在水中存在溶解平衡:
Ca5(PO4)3(OH)?5Ca2++3PO43-+OH-,当F-与Ca2+、PO43-结合生成了更难溶于水的Ca5(PO4)3F,使沉淀平衡向右移动,属于沉淀的转化问题.
故答案为:羟基磷酸钙在水中存在溶解平衡:Ca5(PO4)3(OH)?5Ca2++3PO43-+OH-,当F-与Ca2+、PO43-结合生成了更难溶于水的Ca5(PO4)3F,使上述平衡中Ca2+和PO43-减少而向右移动,继续生成更多的Ca5(PO4)3F,难溶物发生了转化.
(2)第一步反应的方程式,反应物有H2SiF6、和NH4HCO3,生成物有H2SiO3、CO2,根据质量守恒还应有NH4F,则反应的化学方程式为H2SiF6+6NH4HCO3=6NH4F+H2SiO3↓+6CO2↑+3H2O,第二步反应是将第一步生成的NH4F转化为NaF,加入的反应物为NaCl,利用了物质在溶液中溶解度越小则优先析出的特性,所以NaF比NaCl的溶解性小,反应的化学方程式为
NH4F+NaCl=NH4Cl+NaF↓,
故答案为:H2SiF6+6NH4HCO3=6NH4F+H2SiO3↓+6CO2↑+3H2O;NH4F+NaCl=NH4Cl+NaF↓;
(3)操作Ⅱ是将粗NaF洗涤除去其表面的杂质,以得到纯净的NaF,操作Ⅲ是将滤液中的溶质进一步提取,故操作是加热蒸发溶剂,析出大量固体后冷却,
故答案为:除去NaF、NH4Cl 表面的杂质;蒸发浓缩溶液,析出多量固体后冷却;
(4))流程中NH4HCO3必须过量,是指第一步操作中必须保证H2SiF6能全部反应,以防止生成Na2SiF6沉淀,影响制取物质的纯度,
故答案为:保证H2SiF6能全部反应;防止在加入NaCl后H2SiF6与NaCl反应生成Na2SiF6沉淀混入NaF中影响NaF纯度;
(5)从沉淀平衡移动的角度分析,Ca5(PO4)3F的溶解度小于Ca5(PO4)3(OH),羟基磷酸钙在水中存在溶解平衡:
Ca5(PO4)3(OH)?5Ca2++3PO43-+OH-,当F-与Ca2+、PO43-结合生成了更难溶于水的Ca5(PO4)3F,使沉淀平衡向右移动,属于沉淀的转化问题.
故答案为:羟基磷酸钙在水中存在溶解平衡:Ca5(PO4)3(OH)?5Ca2++3PO43-+OH-,当F-与Ca2+、PO43-结合生成了更难溶于水的Ca5(PO4)3F,使上述平衡中Ca2+和PO43-减少而向右移动,继续生成更多的Ca5(PO4)3F,难溶物发生了转化.
点评:本题考查较为综合,题目难度角度,注意把握制备流程的反应原理,根据题中信息解答,本题易错点为相关化学方程式的书写,注意从质量守恒的角度思考.

练习册系列答案
相关题目
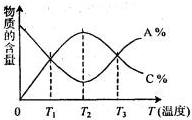 (2009?肇庆二模)经一定时间后,可逆反应aA+bB?cC中物质的含量A%和C%随温度的变化曲线如图所示.下列说法正确的是( )
(2009?肇庆二模)经一定时间后,可逆反应aA+bB?cC中物质的含量A%和C%随温度的变化曲线如图所示.下列说法正确的是( ) 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )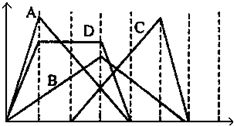 (2009?肇庆二模)下图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量.下列反应对应的曲线错误的是( )
(2009?肇庆二模)下图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量.下列反应对应的曲线错误的是( )