题目内容
13.胆矾CuSO4•5H2O可写成[Cu(H2O)4]SO4•H2O,其结构示意图如下:
(1)下列说法正确的是B(填字母).
A.胆矾所含元素中,H、O、S的半径及电负性依次增大
B.在上述结构示意图中,存在配位键、共价键和离子键
C.胆矾是分子晶体,分子间存在氢键
D.加热条件下胆矾中的水会在相同温度下一同失去
(2)往硫酸铜溶液中加入过量氨水,溶液变为深蓝色,写出所发生反应的离子方程式Cu2++4NH3=[Cu(NH3)4]2+ ;已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是F的电负性比N大,N-F成键电子对向F偏移,导致NF3中N原子核对其孤对电子的吸引能力增强,难以形成配位键,故NF3不易与Cu2+形成配离子.
分析 (1)根据结构示意图中所有氧原子都是饱和氧原子,存在O→Cu配位键,H-O、S-O共价键和Cu、O离子键,胆矾属于离子晶体以及胆矾晶体中水两类,一类是形成配体的水分子,一类是形成氢键的水分子等角度分析;
(2)往硫酸铜溶液中加入过量氨水,溶液变为深蓝色生成四氨合铜离子;根据电负性的角度分析.
解答 解:(1)A.H、O、S分别为第1,2,3周期,所以半径依次增大,但O电负性大于S,故A错误;
B.在上述结构示意图中,存在O→Cu配位键,H-O、S-O共价键和Cu、O离子键,故B正确;
C.胆矾是五水硫酸铜,胆矾是由水合铜离子及硫酸根离子构成的,属于离子晶体,故C错误;
D.由于胆矾晶体中水两类,一类是形成配体的水分子,一类是形成氢键的水分子,结构上有着不同,因此在相同温度不会一同失去,故D错误.
故答案为:B.
(2)往硫酸铜溶液中加入过量氨水,溶液变为深蓝色生成四氨合铜离子,离子方程式为:Cu2++4NH3=[Cu(NH3)4]2+,
N、F、H三种元素的电负性:F>N>H,所以NH3中共用电子对偏向N,而在NF3中,共用电子对偏向F,偏离N原子,
故答案为:Cu2++4NH3=[Cu(NH3)4]2+;F的电负性比N大,N-F成键电子对向F偏移,导致NF3中N原子核对其孤对电子的吸引能力增强,难以形成配位键,故NF3不易与Cu2+形成配离子.
点评 本题考查电负性概念以及离子晶体的晶胞结构、化学键、物质性质、配合物成键状况的了解,题目难度中等,学习中注意加强对晶胞以及晶体结构的分析.

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
4.下列叙述违背化学原理的是( )
| A. | NaHCO3溶液与NaAlO2溶液混合生成白色沉淀,说明结合H+的能力:AlO2->CO32- | |
| B. | 将SO2通入酸性KMnO4溶液中溶液褪色,不能说明SO2具有漂白性 | |
| C. | 工业上制钾的反应为Na+KCl (熔融)=NaCl+K↑,说明还原性Na比K强 | |
| D. | 亚硫酸是良好的还原剂,浓硫酸是良好的氧化剂,但两者混合,却不发生氧化还原反应 |
1.下列有关物质的用途不正确的是( )
| A. | 液氨可用作制冷剂 | B. | SO2广泛用于食品漂白 | ||
| C. | 铁制容器可用于存储浓硝酸 | D. | 浓硫酸不能用来干燥氨气 |
8.不粘锅内壁有一薄层为聚四氟乙烯的高分子材料的涂层,使用不粘锅烧菜时不易粘锅、烧焦.下列关于聚四氟乙烯的说法正确的是( )
| A. | 不粘锅涂层为有机高分子材料,分子中含碳碳双键 | |
| B. | 聚四氟乙烯是由不饱和烃加聚得到的 | |
| C. | 聚四氯乙烯中氟的质量分数为76% | |
| D. | 聚四氟乙烯的化学活动性较强 |
18.生活中有机化合物随处可见.以下生活中提到物质的主要成分不属于高分子化合物的是( )
| A. | 蚕食被中含有的蚕丝 | B. | 大豆油、猪油中含有的油脂 | ||
| C. | 五谷杂粮中含有的淀粉 | D. | 棉质衣服中的纤维素 |
5.已知卤代烃可以和钠发生反应,例如溴乙烷与钠反应为:2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr,应用这一反应,下列所给化合物中可以与钠合成环丁烷的是( )
| A. | CH3CH2Br | B. | CH3CH2CH2CH2Br | ||
| C. | CH2Br CH2CH2Br | D. | CH2Br CH2CH2CH2Br |
2.下列表达正确的是( )
| A. | 羟基的电子式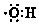 | B. | 醛基的结构简式-COH | ||
| C. | 2-丁烯的键线式  | D. | 2-丙醇的结构简式 C3H7-OH |
4.下列分子的电子式书写正确的是( )
| A. | 双氧水 | B. | 四氯化碳 | C. | 氮气 | D. | 二氧化碳  |
