题目内容
【题目】科学家发现C60分子(图1)由60个碳原子构成,它的形状像足球(图1C),含有C=C键,因此又叫足球烯.1991年科学家又发现一种碳的单质﹣﹣碳纳米管,是由六边环形的碳原子构成的具有很大表面积管状大分子(图1D),图1A、图1B分别是金刚石和石墨的结构示意图.图中小黑点或小黑圈均代表碳原子. 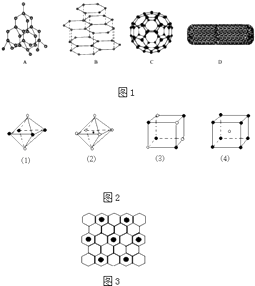
(1)金刚石、石墨、足球烯和碳纳米管四种物质互称为同素异形体,它们在物理性质上存在较大的差异,其原因是;
(2)同条件下,足球烯、石墨分别和气体单质F2反应时,足球烯的化学性质比石墨要活泼,其理由是:;
(3)燃氢汽车之所以尚未大面积推广,除较经济的制氢方法尚未完全解决外,还需解决H2的贮存问题,上述四种碳单质中有可能成为贮氢材料的是:;
(4)图2是从NaCl或CsCl晶体结构图中分割出来的部分结构图,试判断NaCl晶体结构的图象是(填序号);
(5)图1A金刚石结构中一个碳原子被(填数字)个六元环共用;
(6)如图1B,同一层中的原子构成许许多多的正六边形,此单质与熔融的钾单质相互作用,形成某种青铜色的物质(其中的元素钾用“●”表示),原子分布如图3所示,该物质的化学式为
【答案】
(1)碳原子排列方式不同
(2)足球烯含有C=C键容易加成
(3)碳纳米管
(4)(2)(3)
(5)6
(6)KC8
【解析】解:(1)金刚石、石墨、足球烯和碳纳米管四种物质中碳原子在空间的排布方式不同,所以性质会有极大差异; 所以答案是:碳原子排列方式不同; (2)足球烯中含有碳碳双键,所以比石墨活泼,更易于F2发生加成反应;
所以答案是:足球烯含有C=C键容易加成;(3)根据以上各物质的空间结构可知,由于碳纳米管表面积大,可以吸附H2 , 用作贮氢材料;
所以答案是:碳纳米管;(4)氯化钠是6个Na(或Cl)形成的正八面体中间包围一个Cl(或Na),其晶胞是一个正方体,故选(2)(3),(5)金刚石的网状结构中,每个碳原子能形成4个共价键,根据图1A金刚石结构可知,一个碳原子被6个六元环共用,所以答案是:6;(6)如图所示,K原子镶嵌在正六边形的中心,该正六边形周围有6个未镶嵌K原子的C原子正六边形结构,即每正六边形周围连接6个C原子,该碳原子为3个正六边形共有,故结构中K原子与C原子数目之比为1:(6+6× ![]() )=8,故化学式为KC8 ,
)=8,故化学式为KC8 ,
所以答案是:KC8 .

 阅读快车系列答案
阅读快车系列答案

