题目内容
(12分)标况下,在100 mL0.1mol·L-1某NaOH溶液中通入一定量CO2后,再向所得溶液中滴加某浓度的稀盐酸,滴加盐酸的体积与生成气体的情况如图所示。
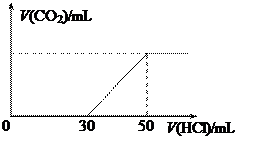
(假设生成的CO2全部逸出)。
求:(1)该稀盐酸物质的量浓度c(HCl)。
(2)滴加稀盐酸至50mL时共产生气体体积。
(3)滴加盐酸前溶液中所含溶质的成分及各自的物质的量浓度。
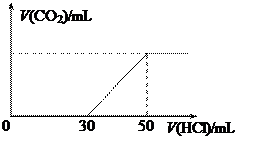
(假设生成的CO2全部逸出)。
求:(1)该稀盐酸物质的量浓度c(HCl)。
(2)滴加稀盐酸至50mL时共产生气体体积。
(3)滴加盐酸前溶液中所含溶质的成分及各自的物质的量浓度。
(1)加入HCl 50mL时,溶液中刚好全生成NaCl
c(HCl)=0.1L×0.1mol·L-1/0.05L=0.2mol·L-1
(2)加入HCl 30mL后,发生的反应为NaHCO3+HCl=NaCl+H2O+CO2 ↑
所以V(CO2)=0.02L×0.2 mol/L×22.4L/mol=0.0896L
(3)从图像可知,第一阶段(无气体产生)耗去30mL盐酸大于
 第二阶段(产生气体并达最大量)耗去的20mL盐酸的体积,可知溶液中溶质的成分只能是NaOH、Na2CO3c(NaOH)=0.02mol·L-1 c(Na2CO3)= 0.04mol·L-1
第二阶段(产生气体并达最大量)耗去的20mL盐酸的体积,可知溶液中溶质的成分只能是NaOH、Na2CO3c(NaOH)=0.02mol·L-1 c(Na2CO3)= 0.04mol·L-1
c(HCl)=0.1L×0.1mol·L-1/0.05L=0.2mol·L-1
(2)加入HCl 30mL后,发生的反应为NaHCO3+HCl=NaCl+H2O+CO2 ↑
所以V(CO2)=0.02L×0.2 mol/L×22.4L/mol=0.0896L
(3)从图像可知,第一阶段(无气体产生)耗去30mL盐酸大于
 第二阶段(产生气体并达最大量)耗去的20mL盐酸的体积,可知溶液中溶质的成分只能是NaOH、Na2CO3c(NaOH)=0.02mol·L-1 c(Na2CO3)= 0.04mol·L-1
第二阶段(产生气体并达最大量)耗去的20mL盐酸的体积,可知溶液中溶质的成分只能是NaOH、Na2CO3c(NaOH)=0.02mol·L-1 c(Na2CO3)= 0.04mol·L-1 略

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
 :无色→红棕色
:无色→红棕色 4:3
4:3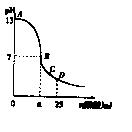
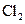 的水溶液可以导电w
的水溶液可以导电w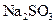 易变质,
易变质,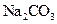 不易变质
不易变质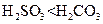
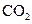 气体出现浑浊
气体出现浑浊