题目内容
(14分)盐酸、硫酸和硝酸都是重要的化工原料,也是化学实验室里必备的重要试剂。请回答下列问题:
(1)常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有 性。用玻璃棒蘸取浓硫酸滴在纸上,纸逐渐变黑,说明浓硫酸具有 性。
(2)硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,工业上用洗净的废铜屑作原料来制备硝酸铜。下列制备方法符合“绿色化学”思想的是 (填序号)。
① Cu + HNO3(浓)→ Cu(NO3)2 ② Cu + HNO3(稀)→ Cu(NO3)2
③ Cu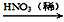 CuO
CuO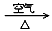 Cu(NO3)2
Cu(NO3)2
(3)①在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,测得产生的气体在标准状况下的体积可能是 。
A.40.32L B.30.24L C.20.16L D.13.44L
②若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式 。
(4)若将12.8g铜跟一定质量的浓HNO3反应,铜消耗完时,共产生气体5.6L(标准状况),则所耗HNO3的物质的量 mol
(5)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水。该反应的化学方程式为 。
(每空2分,共14分)(1)(强)氧化性 脱水性 (2)③
(3)① D ②3Cu + 8H+ + 2NO3- = 3Cu2+ + 2 NO ↑+ 4H2O
(4)0.65 (5) Cu+2HCl+H2O2=CuCl2+2H2O
【解析】(1)常温下,铁和铝再浓硫酸中发生钝化,所以可用铁、铝制的容器盛放浓硫酸,这说明浓硫酸具有强氧化性。又因为浓硫酸还具有脱水性,所以用玻璃棒蘸取浓硫酸滴在纸上,纸逐渐变黑。
(2)在反应①②均可以生成NO或NO2从而污染空气,所以选项①②不正确。在反应③中生成物是硝酸铜和水,不会污染环境,因此答案选③。
(3)①由于随着反应的进行,浓硫酸的浓度会逐渐降低,而稀硫酸与铜是不反应的,所以实际产生的SO2小于理论值,即小于0.9mol×22.4L/mol=20.16L,所以答案选D。
②在硝酸条件下,硝酸盐具有强氧化性,能氧化单质铜,反应的方程式是3Cu + 8H+ + 2NO3- = 3Cu2+ + 2 NO ↑+ 4H2O。
(4)12.8g铜的物质的量是0.2mol,则生成硝酸铜是0.2mol。反应中生成的NO2是0.25mol,所以参加反应的硝酸是0.4mol+0.25mol=0.65mol。
(5)双氧水具有氧化性,能把铜氧化生成铜离子,而双氧水的还原产物是水,所以反应的方程式是Cu+2HCl+H2O2=CuCl2+2H2O。

(14分)盐酸、硫酸和硝酸都是重要的化工原料,也是化学实验室里必备的重要试剂。请回答下列问题:
(1)常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有 性。用玻璃棒蘸取浓硫酸滴在纸上,纸逐渐变黑,说明浓硫酸具有 性。
(2)硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,工业上用洗净的废铜屑作原料来制备硝酸铜。下列制备方法符合“绿色化学”思想的是 (填序号)。
① Cu + HNO3(浓)→ Cu(NO3)2 ② Cu + HNO3(稀)→ Cu(NO3)2
③ Cu CuO
CuO Cu(NO3)2
Cu(NO3)2
(3)①在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,测得产生的气体在标准状况下的体积可能是 。
| A.40.32L | B.30.24L | C.20.16L | D.13.44L |
(4)若将12.8g铜跟一定质量的浓HNO3反应,铜消耗完时,共产生气体5.6L(标准状况),则所耗HNO3的物质的量 mol
(5)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水。该反应的化学方程式为 。
盐酸或硫酸和氢氧化钠溶液的中和反应没有明显的现象。某学习兴趣小组的同学为了证明氢氧化钠溶液与盐酸或硫酸发生了反应,从中和反应的热效应出发,设计了下面几种实验方案。请回答有关问题。
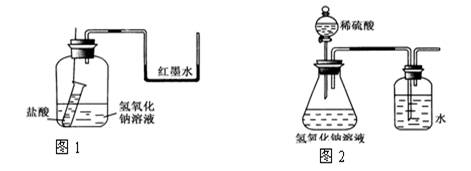
(1)方案一:如图1装好实验装置,图中小试管用细线吊着,细线的上端拴在细铁丝上。开始时使右端U形管两端红墨水相平。实验开始,向下插细铁丝,使小试管内盐酸和广口瓶内氢氧化钠溶液混合,此时观察到的现象是_________ ,原因是___________。
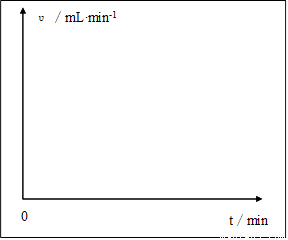
(2)方案二:该小组借助反应溶液温度的变化来判断反应的发生。如果氢氧化钠溶液与盐酸混合前后有温度的变化,则证明发生了化学反应。该小组同学将不同浓度的氢氧化钠溶液和盐酸各10 mL混合,用温度计测量反应前后温度的变化,测得的部分数据如下表:
|
编号 |
盐酸 |
氢氧化钠 |
△t/℃ |
|
1 |
0.1 mol·L-1 |
0.05 mol·L-1 |
3.5 |
|
2 |
0.1 mol·L-1 |
0.1 mol·L-1 |
x |
|
3 |
0.2 mol·L-1 |
0.2 mol·L-1 |
14 |
则x=____________。
(3)方案三:该小组还设计了如图2示装置来证明氢氧化钠溶液确实与稀硫酸发生了反应。他们认为若洗气瓶中导管口有气泡冒出,则说明该反应放出热量,从而证明发生了反应。
①实验时,打开分液漏斗活塞,发现导管流出液体不畅,原因可能是______________
②从原理上讲,该实验设计的不合理之处为__________________________________。
请你在此实验装置的基础上提出修改方案__________________________________。
(14分)某同学利用铁与水蒸气反应后的固体物质进行了如下实验:

(1)固体溶于稀盐酸的化学方程式为 ▲ ;
(2)试剂1的化学式是 ▲ ;加入试剂1后呈红色的原因是(用离子方程式表示): ▲ 。
(3)加入新制氯水后溶液红色加深的原因是(用离子方程式表示) ▲ ;
(4)某一同学在实验中由于加入了过量新制氯水,放置一段时间后,发现深红色褪去,为了探究溶液褪色的原因,另有四位同学进行了下表的猜想,你认为丁同学的猜想会是什么?
|
编 号 |
猜 想 |
|
甲 |
溶液中的+3价Fe又被还原为+2价Fe |
|
乙 |
溶液中的SCN-被过量的氯水氧化 |
|
丙 |
新制的氯水具有漂白性,将该溶液漂白 |
|
丁 |
? |
为验证乙同学的猜想合理与否?请同学们根据结论完成下表的实验设计方案。可选用试剂:浓硫酸、1.0mol·L-1HNO3、1.0mol·L-1盐酸、1.0 mol·L-1 NaOH、0.1mol·L-1FeCl3、0.1mol·L-1CuSO4、20%KSCN、蒸馏水。
|
实验操作 |
预期现象 |
结 论 |
|
|
|
说明乙同学的猜想是合理的 |