��Ŀ����
��2L�ܱ�������ͨ��amol ����A��bmol����B����һ�������·�����Ӧ��xA(g)+yB(g)pC(g)+qD(g)��
��֪��ƽ����Ӧ����vC��1/2vA����Ӧ2min ʱ��A��Ũ�ȼ�����1/3��B�����ʵ���������a/2mol����a mol D���ɡ�
�ش��������⣺
��1����ѧ����ʽ�У�x�� ��y�� ��p�� ��q�� ��
��2����Ӧ2min�ڣ�vA = ��
��3����Ӧƽ��ʱ��DΪ 2amol����B��ת����Ϊ ��
��4����֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�����£�
| �¶ȡ� | 1000 | 1150 | 1300 |
| ƽ�ⳣ�� | 4.0 | 3.7 | 3.5 |
�÷�Ӧ��ƽ�ⳣ������ʽK=_____________����H________0(���������������=��)��
��5����������������䣬���������ݻ���Ϊ1L������ͬ����ʵ�飬����������Ӧ�Ƚϣ�
�ٷ�Ӧ���� �����������С�����䡱�� ��
��ƽ��ʱ��Ӧ���ת���� �����������С�����䡱����������
��
��1��2��3��1��6��4�֣�
��2��a/12 mol��L��1��min��1��2�֣�
��3��a/b��100%��2�֣�
��4��K= c (C)��c 6(D)��c 2(A) ��c 3(B) ��2�֣���<��2�֣�
��5��������1�֣� �ڼ�С��1�֣��������С�������ѹǿ����ƽ��������������ٵķ����淴Ӧ�����ƶ������ʹ��Ӧ��ת���ʼ�С��1�֣�
����:��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д���2L�ܱ�������ͨ��amol ����A��bmol����B����һ�������·�����Ӧ��xA(g)+yB(g) ![]() pC(g)+qD(g)��
pC(g)+qD(g)��
��֪��ƽ����Ӧ����vC��1/2vA����Ӧ2min ʱ��A��Ũ�ȼ�����1/3��B�����ʵ���������a/2mol����a mol D���ɡ�
�ش��������⣺
��1����ѧ����ʽ�У�x�� ��y�� ��p�� ��q�� ��
��2����Ӧ2min�ڣ�vA = ��
��3����Ӧƽ��ʱ��DΪ 2amol����B��ת����Ϊ ��
��4����֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�����£�
| �¶ȡ� | 1000 | 1150 | 1300 |
| ƽ�ⳣ�� | 4.0 | 3.7 | 3.5 |


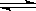 2NH3(g)����֪����Ӧ2min�ﵽƽ�� ����ʱN2��Ũ�ȼ�����2/3��
2NH3(g)����֪����Ӧ2min�ﵽƽ�� ����ʱN2��Ũ�ȼ�����2/3��