��Ŀ����
ϩ������CH2��CH��CH2OH����һ����ɫ�д̼�����ζ��Һ�壬����Ҫ���л��ϳ�ԭ�ϡ���ش�
��1��ϩ�����ķ���ʽΪ ��ϩ�����к��еĹ����ŵ�������____��
��2��0.3mol ϩ���������������Ʒ�Ӧ�������ɱ�״���µ����� __L��
��3��д��ϩ��������ˮ��Ӧ�Ļ�ѧ����ʽ ����Ӧ����Ϊ___________��
��4��ϩ������CH3CO18OH����������Ӧ�Ļ�����ʽΪ ��������Ӧ���ɵIJ�����һ����
���¿��Է����Ӿ۷�Ӧ�õ��߷��ӻ������ṹ��ʽΪ ��
��1��C3H6O(1��) ��̼̼˫�����ǻ�(2��) ��2��3.36 (2��)
��3��CH2��CH��CH2OH+Br2��CH2BrCHBrCH2OH (2��) �� �ӳɷ�Ӧ��1�֣�
��4��CH3CO18O H+CH2��CH��CH2OH  CH3COOCH2CH��CH2+H218O��2�֣�
CH3COOCH2CH��CH2+H218O��2�֣�
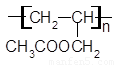 ��2�֣�
��2�֣�
��������
�����������1������ϩ�����Ľṹ��ʽCH2��CH��CH2OH��֪�������ʽΪC3H6O�������к��еĹ�������̼̼˫�����ǻ���
��2��ϩ���������к���1���ǻ���2����ϩ��������1�������������0.3mol ϩ���������������Ʒ�Ӧ���Եõ�0.3mol��2��0.15mol�������ڱ�״���µ������0.15mol��22.4L/mol��3.36L��
��3��ϩ��������̼̼˫�����ܺ���ˮ�����ӳɷ�Ӧ����Ӧ�Ļ�ѧ����ʽΪCH2��CH��CH2OH+Br2��CH2BrCHBrCH2OH��
��4����������Ӧ�������ṩ�ǻ������ṩ��ԭ�ӣ����ϩ������CH3CO18OH����������Ӧ�Ļ�����ʽΪCH3CO18O H+CH2��CH��CH2OH 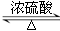 CH3COOCH2CH��CH2+H218O����������������к���̼̼˫�����ܷ����Ӿ۷�Ӧ���ɸ߷��ӻ�������Ը���������Ľṹ��ʽ��֪���õ��ĸ߷��ӻ�����ṹ��ʽΪ
CH3COOCH2CH��CH2+H218O����������������к���̼̼˫�����ܷ����Ӿ۷�Ӧ���ɸ߷��ӻ�������Ը���������Ľṹ��ʽ��֪���õ��ĸ߷��ӻ�����ṹ��ʽΪ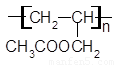 ��
��
���㣺�����л���ṹ�����ʡ��л���Ӧ�����ж��Լ�����ʽ����д��

 ����ͬ�����Ծ�ϵ�д�
����ͬ�����Ծ�ϵ�д�