题目内容
A~H均为短周期元素,A~F在元素周期表中的相对位置如下图所示,G与其它七种元素不在同一周期,H是短周期中原子半径最大的主族元素。由B、G组成的气态化合物甲水溶液呈碱性。
A | B | C |
|
D |
| E | F |
请回答下列问题:
(1)写出甲的电子式,实验室制取气体甲的化学方程式为。
(2)B、C、G个数比为1:1:5形成的化合物的化学键类型为。
A.离子键
B.极性键
C.非极性键
(3)请用电子式表示AE2的形成过程。
(4)用离子符号表示C、E、F、H四种离子的半径由大到小的顺序。
(5)用一个离子方程式解释A比D非金属性强的原因。
练习册系列答案
相关题目
3.运用元素周期律分析下面的推断,其中不正确的是( )
| A. | 硫酸锶(SrSO4)是难溶于水的白色固体 | |
| B. | 砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸 | |
| C. | 在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂 | |
| D. | 硒化氢(H2Se)是有色、有毒的气体,比H2S稳定 |
1.下列属于有机物的是( )
| A. | 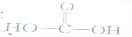 | B. | KSCN | C. | 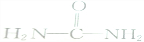 | D. | NH4HCO3 |


 Z(g),经60s达到平衡,生成0.3molZ。下列说法正确的是
Z(g),经60s达到平衡,生成0.3molZ。下列说法正确的是
 碘的流程的一部分
碘的流程的一部分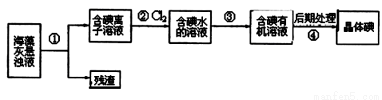
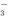 +H+
+H+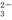 +H2O?HCO
+H2O?HCO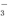 +OH-
+OH-