题目内容
(10分)N2在诸多领域用途广泛。某化学兴趣小组为探究在实验室制备较为纯净N2的方法,进行了认真的准备。请你参与交流与讨论。
【查阅资料】 N2的制法有下列三种方案:
方案1:加热NaNO2和NH4Cl的浓溶液制得N2。
方案2:加热条件下,以NH3还原CuO可制得N2,同时获得活性铜粉。
方案3:将空气缓缓通过灼热的铜粉获得较纯的N2。
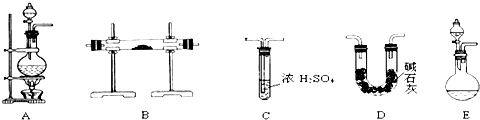
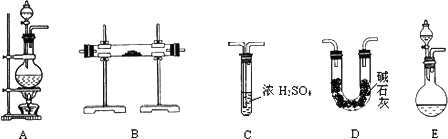
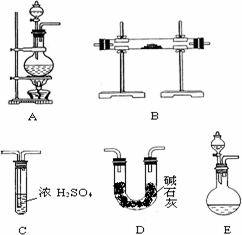
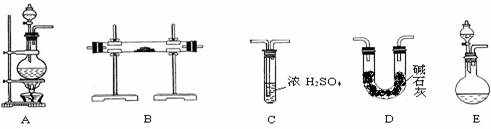
【实验准备】以实验室常见仪器(药品)等设计的部分装置如下图(有的夹持和加热仪器未画出)。
【分析交流】

⑴若以方案1制得N2,应选择的发生装置是 。
⑵若按方案2制得干燥、纯净的N2,且需要的NH3以生石灰和浓氨水作原料,整套制气装置按气流从左到右的顺序连接的顺序是(填写序号,下同) 。获得N2的反应原理是(写反应方程式) 。
⑶若以排水法收集N2,其中会混入水蒸气。但也不宜用排空气法,其原因是 。你提出的收集方法是 。
⑷上述三个方案中,制得的N2纯度最差的是 。在N2纯度要求不甚严格的情况下,有人建议将方案2和方案3结合使用,你认为其优点是 。
⑴A(1分)
⑵E→D→B→C(2分);2NH3+3CuO===3Cu+N2↑+3H2O(方程式没配平为1分,2分)。
⑶N2的相对分子质量28与空气的平均相对分子质量相近(1分,用气体密度大小比较回答问题也给分)。以塑料袋直接收集(1分,其他合理答案也给分)。
⑷方案3(1分);CuO和Cu可循环反复利用,节省药品(2分)。