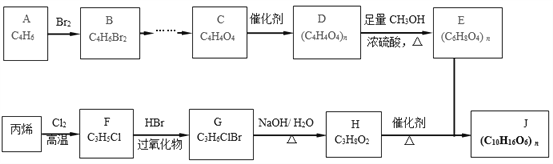
题目内容
【题目】下列化学用语正确的是
A. NaHCO3的水解:HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
B. 醋酸的电离:CH3COOH=CH3COO-+H+
C. 碳酸钙的溶解平衡:CaCO3(s)![]() Ca2+(aq)+CO32-(aq)
Ca2+(aq)+CO32-(aq)
D. H2的燃烧热为285.8 kJ/mol,则表示H2燃烧热的热化学方程式为:H2(g)+1/2O2(g)=H2O(g) ΔH=-285.8 kJ/mol
【答案】C
【解析】A.NaHCO3的水解反应式:HCO3-+H2O![]() H2CO3+OH-,故A错误;B.醋酸是弱酸,其电离方程式为CH3COOH
H2CO3+OH-,故A错误;B.醋酸是弱酸,其电离方程式为CH3COOH![]() CH3COO-+H+,故B错误;C.碳酸钙在水溶液中存在的溶解平衡为CaCO3(s)
CH3COO-+H+,故B错误;C.碳酸钙在水溶液中存在的溶解平衡为CaCO3(s)![]() Ca2+(aq)+CO32-(aq),故B正确;D.1molH2完全燃烧生成液态水时放出的热量称为燃烧热,则表示H2燃烧热的热化学方程式为:H2(g)+1/2O2(g)=H2O(l) ΔH=-285.8 kJ/mol ,故D错误;答案为C。
Ca2+(aq)+CO32-(aq),故B正确;D.1molH2完全燃烧生成液态水时放出的热量称为燃烧热,则表示H2燃烧热的热化学方程式为:H2(g)+1/2O2(g)=H2O(l) ΔH=-285.8 kJ/mol ,故D错误;答案为C。

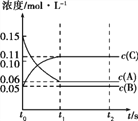
【题目】Ⅰ.拆开1mol气态物质中某种共价键需要吸收的能量,就是该共价键的键能。下表是某些共价键的键能:根据右图中能量变化图,回答下列问题:
(1)图中:a=___________。
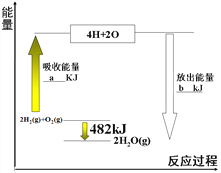
(2)表格中:X=__________。
共价键 | H-H | O=O | H-O |
键能/kJ ·mol-1 | 436 | 498 | X |
Ⅱ.如图,A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
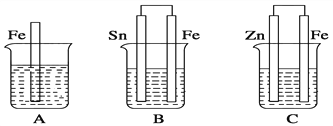
(1)A中反应的离子方程式为_____________________________。
(2)B中Sn极的电极反应式为____________________________。
(3)C中被腐蚀的金属是________,总反应的化学方程式为_________________________,
比较A、B、C中铁被腐蚀的速率,由快到慢的顺序为__________(填序号)。
【题目】下列实验中,所采取的分离方法不正确的是( )
选项 | 目的 | 分离方法 |
A | 除去铜器表面的铜绿[Cu2(OH)2CO3] | 用盐酸浸泡,再用清水冲洗 |
B | 除去乙醇中的少量水 | 加生石灰,再蒸馏 |
C | 除去氯化铁中含有少量氯化亚铁杂质 | 加入溴水 |
D | 除去NaCl固体中的NH4Cl | 加热 |
A.A
B.B
C.C
D.D