题目内容
三氟化氮(NF3)是微电子工业中一种优良的等离子蚀刻气体。它无色、无臭,在潮湿的空气中能发生下列反应:3NF3+5H2O 2NO+HNO3+9HF,下列有关说法正确的是( )
2NO+HNO3+9HF,下列有关说法正确的是( )
A.反应中NF3是氧化剂,H2O是还原剂
B.反应中被氧化与被还原的原子物质的量之比为2∶1
C.若反应中生成0.2 mol HNO3,则反应共转移0.2 mol e-
D.NF3在潮湿的空气中泄漏会产生白雾、红棕色气体等现象
D
【解析】NF3中N是+3价,F是-1价,HNO3中N是+5价,故此反应是歧化反应,被氧化与被还原的原子都是N,画出双线桥,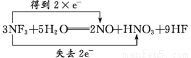 就可以得出反应中NF3既是氧化剂又是还原剂,H2O既不是氧化剂也不是还原剂;反应中被氧化与被还原的原子物质的量之比为1∶2;若反应中生成0.2 mol HNO3,则反应共转移0.4 mol e-,由题给方程式知,白雾是由HF形成的,红棕色气体是由NO氧化成NO2所致。
就可以得出反应中NF3既是氧化剂又是还原剂,H2O既不是氧化剂也不是还原剂;反应中被氧化与被还原的原子物质的量之比为1∶2;若反应中生成0.2 mol HNO3,则反应共转移0.4 mol e-,由题给方程式知,白雾是由HF形成的,红棕色气体是由NO氧化成NO2所致。

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目