题目内容
在酸性介质中,往MnSO4溶液里滴加(NH4)2S2O8(过二硫酸铵)溶液会发生如下反应:Mn2++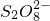 +H2O→MnO4-+
+H2O→MnO4-+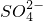 +H+,下列说法不正确的是
+H+,下列说法不正确的是
- A.可以利用该反应检验Mn2+
- B.氧气性比较:S2O82->MnO4-
- C.该反应中酸性介质可以为盐酸
- D.若有0.1mol氧化产物生成,则转移电子0.5mol
C
分析:A.酸性条件下,锰离子能被过二硫酸根离子氧化生成高锰酸根离子,高锰酸根离子呈紫色;
B.同一化学反应中,氧化剂的氧化性大于氧化产物的氧化性;
C.盐酸为强还原性酸,能被过二硫酸根离子氧化;
D.根据氧化产物和转移电子之间的关系式计算转移电子数.
解答:A.酸性条件下,锰离子能被过二硫酸根离子氧化生成高锰酸根离子,锰离子无色,高锰酸根离子呈紫色,所以可以用该反应检验Mn2+,故A正确;
B.该反应中,过二硫酸根离子得电子化合价降低为氧化剂,锰离子失电子化合价升高为还原剂,则高锰酸根离子为氧化产物,氧化剂的氧化性大于氧化产物的氧化性,所以氧化性比较:S2O82->MnO4-,故B正确;
C.盐酸为强还原性酸,能被过二硫酸根离子氧化生成氯气,所以不能用盐酸作酸性介质,故C错误;
D.Mn2++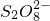 +H2O→MnO4-+
+H2O→MnO4-+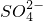 +H+转移电子
+H+转移电子
1mol 5mol
0.1mol 0.5mol
所以若有0.1mol氧化产物生成,则转移电子0.5mol,故D正确;
故选C.
点评:本题考查了氧化还原反应,明确元素化合价是解本题的关键,注意盐酸是强酸且是强还原性酸,易被强氧化剂氧化,为易错点.
分析:A.酸性条件下,锰离子能被过二硫酸根离子氧化生成高锰酸根离子,高锰酸根离子呈紫色;
B.同一化学反应中,氧化剂的氧化性大于氧化产物的氧化性;
C.盐酸为强还原性酸,能被过二硫酸根离子氧化;
D.根据氧化产物和转移电子之间的关系式计算转移电子数.
解答:A.酸性条件下,锰离子能被过二硫酸根离子氧化生成高锰酸根离子,锰离子无色,高锰酸根离子呈紫色,所以可以用该反应检验Mn2+,故A正确;
B.该反应中,过二硫酸根离子得电子化合价降低为氧化剂,锰离子失电子化合价升高为还原剂,则高锰酸根离子为氧化产物,氧化剂的氧化性大于氧化产物的氧化性,所以氧化性比较:S2O82->MnO4-,故B正确;
C.盐酸为强还原性酸,能被过二硫酸根离子氧化生成氯气,所以不能用盐酸作酸性介质,故C错误;
D.Mn2++
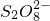 +H2O→MnO4-+
+H2O→MnO4-+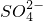 +H+转移电子
+H+转移电子1mol 5mol
0.1mol 0.5mol
所以若有0.1mol氧化产物生成,则转移电子0.5mol,故D正确;
故选C.
点评:本题考查了氧化还原反应,明确元素化合价是解本题的关键,注意盐酸是强酸且是强还原性酸,易被强氧化剂氧化,为易错点.

练习册系列答案
相关题目
化学学习中,有关物质性质的学习离不开实验,请阅读下列对应的内容,并按要求完成填空
(1)实验室经常用烧杯进行性质实验研究,如用图1所示装置及下表中试剂,过一段时间实验1、2、3、4烧杯①中的现象分别是______,______,______,______,
| 实验编号 | ①中的物质 | ②中的物质 |
| 1 | 淀粉碘化钾溶液 | 浓硝酸 |
| 2 | 酚酞溶液 | 浓硫酸 |
| 3 | 氯化铝溶液 | 浓氨水 |
| 4 | 湿润的红纸 | 饱和氯水 |
(3)浓氨水通常可以用于实验室快速制取氨气及其相关实验的探究,回答下列问题.

①若要测定生成的NH3的体积,则必须选择的装置是______(填装置序号),装置中所盛试剂应具有的性质是______.收集干燥的NH3,收集装置应选择(填装置序号)______,理由是______.
②向浓CaCl2溶液中先通入NH3再通入CO2气体可制纳米级(粒子直径在1-10nm之间)碳酸钙,试写出制纳米级碳酸钙的离子方程式______.
(4)图3是苯与溴发生反应并进行产物检验的反应装置实验装置中的冷凝管“左低右高”的放置目的是______,整套实验装置中能防止倒吸的装置是______(填装置序号)
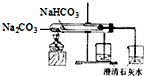
对于固体硫化钠露置在空气中的变化,有如下假设:
假设①:固体硫化钠易被空气中的氧气氧化为单质硫.
假设②:固体硫化钠易被空气中的氧气氧化为亚硫酸钠.
假设③:固体硫化钠易被空气中的氧气氧化为硫酸钠.
为了探究固体硫化钠露置在空气中究竟有怎样的变化,某化学学习小组进行了如下实验:
①从试剂瓶中取出固体硫化钠样品,放在研钵中研碎.
②将研钵中的样品露置在空气中两天.
③从研钵中取出一药匙样品放在试管中,加入盐酸,试样全部溶解,得到澄清溶液,并放出大量气泡.
④立即加塞,用力振荡,产生浑浊,且气泡的量大大减少.
(5)解释加塞振荡后产生浑浊,且气泡大量减少的原因(用化学方程式表示)______.
(6)如果要验证③是否成立的实验方法是______.