题目内容
某气态烃对空气的相对密度为2,在氧气中完全燃烧1.16g这种烃,测得生成1.8g水和3.52g二氧化碳,求这种烃的化学式.
答案:
解析:
解析:
|
解:根据阿伏加德罗定律可知,该烃的摩尔质量=29×2=58(g/mol) 因为:1.16 g该烃的物质的量= 1.8 g水中含氢元素物质的量= 3.52 g二氧化碳中含碳元素物质的量= 所以:0.02∶0.08∶0.2=1∶4∶10 则1 mol该烃含碳元素 4 mol,氢元素 10 mol,化学式为 |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 =0.02(mol)
=0.02(mol) ×2=0.2(mol)
×2=0.2(mol)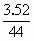 ×1=0.08(mol)
×1=0.08(mol)