题目内容
(2014届四川省眉山市高三第一次诊断性考试化学试卷)
根据Mg能在CO2中燃烧,某兴趣小组推测Na应该也能在CO2中燃烧,且固体产物可能为C、Na2O和Na2CO3中的两种或三种。该小组用如下图装置进行了实验探究。已知PdCl2能被CO还原得到黑色的Pd。

回答下列问题:
(1)为了使反应随开随用,随关随停,上图虚线方框内应选用 装置(填下图字母代号),如何检验所选装置的气密性 。

(2)装置2中所盛试剂为 。
A.NaOH溶液 B.饱和NaHCO3溶液
C.饱和Na2CO3溶液 D.饱和NaCl溶液
(3)检测装置的气密性完好并装好药品后,在点燃酒精灯前应先进行装置1中的反应操作,待观察到 现象时,再点燃酒精灯,这步操作的目的是 。
(4)由实验现象和进一步的探究得出反应机理。
A.装置6中有黑色沉淀生成;
B.取反应后直玻管中的固体物质23.0g溶于足量的水中,无气泡产生且得到澄清的溶液;将溶液加水稀释配成250 mL的溶液;
C.取25.00ml步骤B的溶液,滴加足量BaCl2溶液,将生成的白色沉淀过滤、洗涤、干燥,称量得固体质量为1.97g。
①步骤C中不溶物干燥前必须经过洗涤,如何检验该沉淀是否洗涤干净 。
②该探究得出钠与二氧化碳反应的化学方程式为 。
根据Mg能在CO2中燃烧,某兴趣小组推测Na应该也能在CO2中燃烧,且固体产物可能为C、Na2O和Na2CO3中的两种或三种。该小组用如下图装置进行了实验探究。已知PdCl2能被CO还原得到黑色的Pd。

回答下列问题:
(1)为了使反应随开随用,随关随停,上图虚线方框内应选用 装置(填下图字母代号),如何检验所选装置的气密性 。

(2)装置2中所盛试剂为 。
A.NaOH溶液 B.饱和NaHCO3溶液
C.饱和Na2CO3溶液 D.饱和NaCl溶液
(3)检测装置的气密性完好并装好药品后,在点燃酒精灯前应先进行装置1中的反应操作,待观察到 现象时,再点燃酒精灯,这步操作的目的是 。
(4)由实验现象和进一步的探究得出反应机理。
A.装置6中有黑色沉淀生成;
B.取反应后直玻管中的固体物质23.0g溶于足量的水中,无气泡产生且得到澄清的溶液;将溶液加水稀释配成250 mL的溶液;
C.取25.00ml步骤B的溶液,滴加足量BaCl2溶液,将生成的白色沉淀过滤、洗涤、干燥,称量得固体质量为1.97g。
①步骤C中不溶物干燥前必须经过洗涤,如何检验该沉淀是否洗涤干净 。
②该探究得出钠与二氧化碳反应的化学方程式为 。
(1)C(2分),关闭弹簧夹,向长颈漏斗中加水,一定时间后静置液面保持不动,说明气密性良好(2分)
(2)B(2分)
(3)装置5中出现大量混浊(2分);排尽装置中的空气(2分)
(4)①取最后一次洗涤液加入稀H2SO4,不出现浑浊说明沉淀洗涤干净(2分)
②6Na+4CO2 2Na2O+Na2CO3+3CO(2分)
2Na2O+Na2CO3+3CO(2分)
(2)B(2分)
(3)装置5中出现大量混浊(2分);排尽装置中的空气(2分)
(4)①取最后一次洗涤液加入稀H2SO4,不出现浑浊说明沉淀洗涤干净(2分)
②6Na+4CO2
 2Na2O+Na2CO3+3CO(2分)
2Na2O+Na2CO3+3CO(2分)C装置是采用固液分开的设计,打开弹簧夹液体加入反应开始,关闭弹簧夹反应产生气体的压强使固液分开反应停止;检验有多个出口的实验装置的气密性,一般只保留一个封住其它出口进行实验,关闭弹簧夹,向长颈漏斗中加水,一定时间后静置液面保持不动,说明气密性良好;(2)装置C是用石灰石或大理石与盐酸反应产生二氧化碳,会混有HCl杂质,故2用饱和NaHCO3溶液来除去HCl同时转化为二氧化碳;(3)CO易燃,混有空气可能会发生爆炸,反应前需先同二氧化碳除去装置中的空气,当观察到5中石灰水变浑浊时认为装置中充满二氧化碳,空气排尽;(4)检验洗涤是否干净,一般是要取最后次的洗涤液,进行检验可能存在的杂质离子,鉴于洗涤液中离子浓度较低,一般检验比较容易出现现象的离子如硫酸根离子、氯离子等;
根据实验现象知产物物碳单质,无钠剩余,根据碳酸钡的质量计算出
n(Na2CO3)= n(BaCO3)=1.97÷197×10=0.1mol
m(Na2CO3)= 0.1×106=10.6g
所以固体中含有氧化钠n(Na2O)=(23.0-10.6)÷62=0.2mol
根据氧化还原反应原理,反应中碳元素化合价下降为+2价CO,方程式为
6Na+4CO2
 2Na2O+Na2CO3+3CO
2Na2O+Na2CO3+3CO
练习册系列答案
相关题目
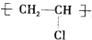 )有毒,不能用于制作食品保鲜袋.由氯乙烯通过加聚反应获得聚氯乙烯的化学方程式为:______.
)有毒,不能用于制作食品保鲜袋.由氯乙烯通过加聚反应获得聚氯乙烯的化学方程式为:______.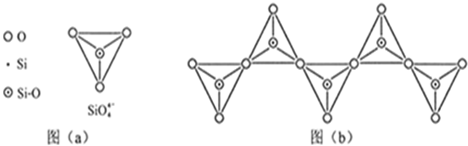
 SiHCl3+H2);
SiHCl3+H2);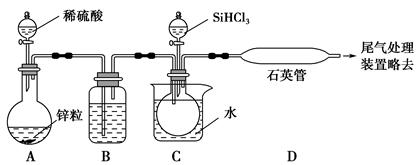
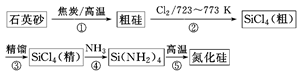
 Si3N4(s)+12HCl(g) ΔH=a kJ/mol(a<0)
Si3N4(s)+12HCl(g) ΔH=a kJ/mol(a<0)