题目内容
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。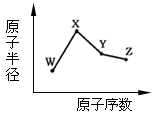
下列说法正确的是
| A.对应简单离子半径:Z>X>W |
| B.对应气态氢化物的稳定性Y>Z |
| C.化合物XZW既含离子键,又含共价键 |
| D.Y的氧化物既能与Z的氢化物溶液反应,又能与X的最高价氧化物对应水化物的溶液反应 |
C
解析试题分析:W的一种核素的质量数为18,中子数为10,则W为O元素,X和Ne原子的核外电子数相差1,且半径比O大,故X为Na元素,Y的单质是一种常见的半导体材料为Si,Z的非金属性在同周期元素中最强应为Cl;故A、对应简单离子半径应为:Z>W>X;B、对应气态氢化物的稳定性应为Z>Y;C、化合物XZW为NaClO中既含离子键,又含共价键,正确;D、Y的氧化物为SiO2,不可与HCl反应,D错误。
考点:考查原子结构与性质、化学键等相关知识。

四种主族元素的离子a Xm+,bYn+,cZn-和dRm-(a,b,c,d为元素的原子序数),它们具有相同的电子层结构,若m>n,对下列叙述的判断正确的是( )
①a-b=n-m ②元素的原子序数a>b>c>d
③元素非金属性Z>R ④最高价氧化物对应水化物碱性X>Y
| A.②③正确 | B.只有③正确 | C.①②③④正确 | D.①②③正确 |
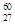 Co是r射线的放射源,关于
Co是r射线的放射源,关于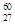 27Co的说法正确的是
27Co的说法正确的是
| A.质子数为 33 | B.中子数为27 | C.质量数为60 | D.核电荷数为60 |
有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数)。下列说法正确的是
| A.若X(OH)n为强碱,则Y(OH)n也一定为强碱 |
| B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性 |
| C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2 |
| D.若Y的最高正价为+m,则X的最高正价一定为+m |
X元素的阳离子和Y元素的阴离子具有和氩原子相同的电子层结构,下列叙述正确的是( )
| A.X的原子序数比Y的小 | B.X 原子的最外层电子数比Y的大 |
| C.X的原子半径比Y的大 | D.X元素的最高正价比Y的小 |
短周期主族元素X、Y、Z、W的原子序数依次增大。X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族。下列说法正确的是
| A.原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) |
| B.Y分别与Z、W形成的化合物中化学键类型相同 |
| C.X的最高价氧化物对应水化物的酸性比W的弱 |
| D.Y的气态简单氢化物的热稳定性比W的强 |
X、Y、Z是短周期的三种主族元素,在周期表中的相对位置如图所示,下列说法正确的是
| X | |
| Y | Z |
A.原子半径:X<Y<Z
B.X、Y、Z三种元素的最高价氧化物对应水化物中最多有一种强酸
C.X的气态氢化物的稳定性比Y的气态氢化物强
D.常温下X、Y、Z的单质不可能均与盐酸反应
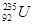 是重要的核工业原料,但在自然界的丰度很低,
是重要的核工业原料,但在自然界的丰度很低,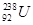 互为同位素
互为同位素