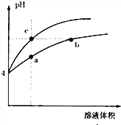
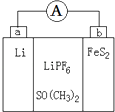
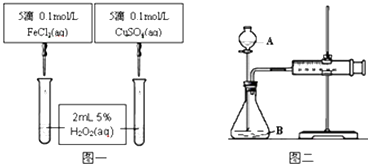
题目内容
【题目】请回答:
(1)H2O2的电子式 .
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由 .
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式 .
(4)完成以下氧化还原反应的离子方程式:
MnO4﹣+C2O42﹣+=Mn2+CO2↑+ .
【答案】
(1)![]()
(2)2Mg+CO2 ![]() 2MgO+C
2MgO+C
(3)Br﹣+AgCl?AgBr+Cl﹣
(4)2;5;16H+;2;10;8H2O
【解析】解:(1.)为共价化合物,结构式为H﹣O﹣O﹣H,其电子式为 ![]() ,所以答案是:
,所以答案是: ![]() ;
;
(2.)镁燃烧不能用CO2灭火,二者反应生成MgO和C,反应为2Mg+CO2 ![]() 2MgO+C所以答案是:2Mg+CO2
2MgO+C所以答案是:2Mg+CO2 ![]() 2MgO+C;
2MgO+C;
(3.)白色沉淀转化为淡黄色沉淀,发生沉淀的转化,AgCl转化为AgBr,离子反应为Br﹣+AgClAgBr+Cl﹣ , 所以答案是:Br﹣+AgClAgBr+Cl﹣;
(4.)Mn元素的化合价由+7价降低为+2价,C元素的化合价由+3价升高为+4价,则由电子守恒可知2MnO4﹣+5 C2O42﹣+→2Mn2+10 CO2↑+,由电荷守恒可知2MnO4﹣+5 C2O42﹣+16H+→2Mn2+10 CO2↑+,由原子守恒可知2MnO4﹣+5 C2O42﹣+16H+=2Mn2+10 CO2↑+8H2O所以答案是:2;5;16H+;2;10;8H2O.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目