题目内容
将铁粉和硫粉混合后加热,待反应一发生即停止加热,反应仍可持续进行,直至反应完全生成新物质硫化亚铁.这现象说明了
- A.该反应是吸热反应
- B.该反应是非氧化还原反应
- C.铁粉和硫粉在常温下难以发生反应
- D.硫化亚铁的总能量高于铁粉和硫粉的总能量
C
分析:根据反应一发生即停止加热,反应仍可持续进行来判断,该反应为放热反应,反应中Fe、S元素的化合价均发生变化,结合反应需要加热才能发生及反应物和生成物的能量高低与放热反应来分析.
解答:A.停止加热,反应仍可持续进行来判断,该反应为放热反应,故A错误;
B.反应中Fe、S元素的化合价均发生变化,属于氧化还原反应,故B错误;
C.该反应常温下不进行,需要加热才反应,故C正确;
D.因反应为放热反应,则硫化亚铁的总能量低于铁粉和硫粉的总能量,故D错误;
故选C.
点评:本题主要考查的是物质发生化学变化时的能量变化及反应现象和本质的联系等知识点,侧重学生分析解决问题能力的考查,题目难度不大.
分析:根据反应一发生即停止加热,反应仍可持续进行来判断,该反应为放热反应,反应中Fe、S元素的化合价均发生变化,结合反应需要加热才能发生及反应物和生成物的能量高低与放热反应来分析.
解答:A.停止加热,反应仍可持续进行来判断,该反应为放热反应,故A错误;
B.反应中Fe、S元素的化合价均发生变化,属于氧化还原反应,故B错误;
C.该反应常温下不进行,需要加热才反应,故C正确;
D.因反应为放热反应,则硫化亚铁的总能量低于铁粉和硫粉的总能量,故D错误;
故选C.
点评:本题主要考查的是物质发生化学变化时的能量变化及反应现象和本质的联系等知识点,侧重学生分析解决问题能力的考查,题目难度不大.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
细菌冶金是一种新工艺,其能耗少、减少环境污染.称为“绿色冶金”.其原理:①氧化硫硫杆菌和聚硫杆菌能把矿石中的硫氧化成硫酸,反应式为2S+3O2+2H2O═2H2SO4,②氧化亚铁硫杆菌在上面产生的硫酸中能把硫酸亚铁氧化成硫酸铁③细菌得到了所需要的能量,生成的硫酸铁可把FeS2(黄铁矿)和Cu2S(辉铜矿)等转变为可溶性化合物而从矿石中溶解出来,其化学过程是:
Fe2S2(黄铁矿)+7Fe2(SO4)3+8H2O═15FeSO4+8H2SO4
Cu2S(辉铜矿)+2Fe2(SO4)2═2CuSO4+4FeSO4+S
(1)写出②反应的化学方程式:______.
(2)某实验小组,欲将硫酸铜和硫酸亚铁的酸性混合液分离出硫酸亚铁溶液.经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如表2
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
实验经过滤后还需设计的实验操作步骤和目的是:
| 实验步骤 | 实验操作 | 实验操作的目的 |
| 步骤1 | ______ | ______ |
| 步骤2 | ______ | ______ |
| 步骤3 | ______ | ______ |
| 步骤4 | 洗涤 | ______ |
| 步骤5 | ______ | 得到FeSO4溶液 |
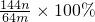 .该学生的计算是否正确:______,请说明理由______.
.该学生的计算是否正确:______,请说明理由______.
细菌冶金是一种新工艺,其能耗少、减少环境污染.称为“绿色冶金”.其原理:①氧化硫硫杆菌和聚硫杆菌能把矿石中的硫氧化成硫酸,反应式为2S+3O2+2H2O═2H2SO4,②氧化亚铁硫杆菌在上面产生的硫酸中能把硫酸亚铁氧化成硫酸铁③细菌得到了所需要的能量,生成的硫酸铁可把FeS2(黄铁矿)和Cu2S(辉铜矿)等转变为可溶性化合物而从矿石中溶解出来,其化学过程是:
Fe2S2(黄铁矿)+7Fe2(SO4)3+8H2O═15FeSO4+8H2SO4
Cu2S(辉铜矿)+2Fe2(SO4)2═2CuSO4+4FeSO4+S
(1)写出②反应的化学方程式: .
(2)某实验小组,欲将硫酸铜和硫酸亚铁的酸性混合液分离出硫酸亚铁溶液.经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如表2
实验室有下列试剂可供选择A. H2O2 B.CaO C.CuO D.稀H2SO4 E.铁粉;
实验经过滤后还需设计的实验操作步骤和目的是:
(3)若向CuSO4、FeSO4混合液中加入适量碱液,将溶液蒸干、灼烧得到红色粉末是Fe2O3、Cu2O混合物,欲测定该混合物中Cu2O的质量分数.该实验小组的方法是向m g混合物中加人足量的稀硫酸,经过滤、洗涤、干燥、称量固体的质量为n g.已知Cu2O溶于稀硫酸生成Cu和CuSO4.某学生据此计算出该混合物Cu2O的质量分数的计算式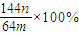 .该学生的计算是否正确: ,请说明理由 .
.该学生的计算是否正确: ,请说明理由 .
Fe2S2(黄铁矿)+7Fe2(SO4)3+8H2O═15FeSO4+8H2SO4
Cu2S(辉铜矿)+2Fe2(SO4)2═2CuSO4+4FeSO4+S
(1)写出②反应的化学方程式: .
(2)某实验小组,欲将硫酸铜和硫酸亚铁的酸性混合液分离出硫酸亚铁溶液.经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如表2
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
实验经过滤后还需设计的实验操作步骤和目的是:
| 实验步骤 | 实验操作 | 实验操作的目的 |
| 步骤1 | ||
| 步骤2 | ||
| 步骤3 | ||
| 步骤4 | 洗涤 | |
| 步骤5 | 得到FeSO4溶液 |
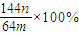 .该学生的计算是否正确: ,请说明理由 .
.该学生的计算是否正确: ,请说明理由 .
细菌冶金是一种新工艺,其能耗少、减少环境污染.称为“绿色冶金”.其原理:①氧化硫硫杆菌和聚硫杆菌能把矿石中的硫氧化成硫酸,反应式为2S+3O2+2H2O═2H2SO4,②氧化亚铁硫杆菌在上面产生的硫酸中能把硫酸亚铁氧化成硫酸铁③细菌得到了所需要的能量,生成的硫酸铁可把FeS2(黄铁矿)和Cu2S(辉铜矿)等转变为可溶性化合物而从矿石中溶解出来,其化学过程是:
Fe2S2(黄铁矿)+7Fe2(SO4)3+8H2O═15FeSO4+8H2SO4
Cu2S(辉铜矿)+2Fe2(SO4)2═2CuSO4+4FeSO4+S
(1)写出②反应的化学方程式: .
(2)某实验小组,欲将硫酸铜和硫酸亚铁的酸性混合液分离出硫酸亚铁溶液.经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如表2
实验室有下列试剂可供选择A. H2O2 B.CaO C.CuO D.稀H2SO4 E.铁粉;
实验经过滤后还需设计的实验操作步骤和目的是:
(3)若向CuSO4、FeSO4混合液中加入适量碱液,将溶液蒸干、灼烧得到红色粉末是Fe2O3、Cu2O混合物,欲测定该混合物中Cu2O的质量分数.该实验小组的方法是向m g混合物中加人足量的稀硫酸,经过滤、洗涤、干燥、称量固体的质量为n g.已知Cu2O溶于稀硫酸生成Cu和CuSO4.某学生据此计算出该混合物Cu2O的质量分数的计算式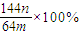 .该学生的计算是否正确: ,请说明理由 .
.该学生的计算是否正确: ,请说明理由 .
Fe2S2(黄铁矿)+7Fe2(SO4)3+8H2O═15FeSO4+8H2SO4
Cu2S(辉铜矿)+2Fe2(SO4)2═2CuSO4+4FeSO4+S
(1)写出②反应的化学方程式: .
(2)某实验小组,欲将硫酸铜和硫酸亚铁的酸性混合液分离出硫酸亚铁溶液.经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如表2
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
实验经过滤后还需设计的实验操作步骤和目的是:
| 实验步骤 | 实验操作 | 实验操作的目的 |
| 步骤1 | ||
| 步骤2 | ||
| 步骤3 | ||
| 步骤4 | 洗涤 | |
| 步骤5 | 得到FeSO4溶液 |
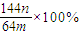 .该学生的计算是否正确: ,请说明理由 .
.该学生的计算是否正确: ,请说明理由 .