题目内容
【题目】亚铁氰化钾K4Fe(CN)6俗名黄血盐,可溶于水,不溶于乙醇。以某电镀厂排放的含NaCN废液为主要原料制备黄血盐的流程如下:
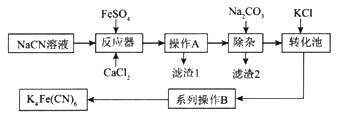
请回答下列问题:
(1)常温下,HCN的电离常数Ka=6.2×10-10。
①实验室配制一定浓度的NaCN溶液时,将NaCN溶解于一定浓度的NaOH溶液中,加水稀释至指定浓度,其操作的目的是_____________。
②浓度均为0.5 mol/L的NaCN和HCN的混合溶液显_________(填“酸”“碱”或“中”)性,通过计算说明:___________________________________。
(2)滤渣1的主要成分是______________(填化学式)。
(3)转化池中发生复分解反应生成K4Fe(CN)6,说明该反应能发生的理由:_____________。
(4)系列操作B为_________________。
(5)实验室中,K4Fe(CN)6可用于检验Fe3+,生成的难溶盐KFe[Fe(CN)6]可用于治疗Tl2SO4中毒,试写出上述治疗Tl2SO4中毒的离子方程式:_______________。
(6)一种太阳能电池的工作原理如图所示,电解质为铁氰化钾K3Fe(CN)6和亚铁氰化钾K4Fe(CN)6的混合溶液。
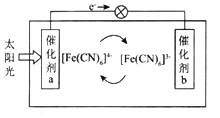
①K+移向催化剂____________(填“a”或“b”)。
②催化剂a表面发生的反应为____________________。
【答案】 抑制![]() 水解 碱
水解 碱 ![]() ,即水解平衡常数大于电离平衡常数,所以溶液呈碱性
,即水解平衡常数大于电离平衡常数,所以溶液呈碱性 ![]() 相同温度下
相同温度下![]() 的溶解度小于
的溶解度小于![]() 过滤、洗涤、干燥
过滤、洗涤、干燥 ![]() b
b ![]()
【解析】由流程可知,NaCN废液中加入硫酸亚铁、氯化钙,发生6NaCN+FeSO4+CaCl2=Na4[Fe(CN)6+CaSO4↓+2NaCl,然后加入碳酸钠溶液可除去过量的Ca2+,经过滤后在滤液中加入KCl可转化生成K4[Fe(CN)6,说明K4[Fe(CN)6溶解度较小。
(1)①根据HCN的电离常数Ka=6.2×10-10可知,HCN为弱酸,NaCN溶液能够水解显碱性,实验室配制一定浓度的NaCN溶液时,将NaCN溶解于一定浓度的NaOH溶液中,可以抑制![]() 水解,故答案为:抑制
水解,故答案为:抑制![]() 水解;
水解;
②根据Kh=![]() 可知,Kh=
可知,Kh=![]() =
=![]() =
=![]() =
=![]() =1.6×10-5>6.2×10-10,即水解平衡常数大于电离平衡常数,所以溶液呈碱性,故答案为:碱;Kh=
=1.6×10-5>6.2×10-10,即水解平衡常数大于电离平衡常数,所以溶液呈碱性,故答案为:碱;Kh=![]() =
=![]() =
=![]() =
=![]() =1.6×10-5>6.2×10-10;
=1.6×10-5>6.2×10-10;
(2)由流程可知,NaCN废液中加入硫酸亚铁、氯化钙,发生6NaCN+FeSO4+CaCl2=Na4[Fe(CN)6+CaSO4↓+2NaCl,滤渣1的主要成分是CaSO4,故答案为:CaSO4;
(3)相同温度下![]() 的溶解度小于
的溶解度小于![]() ,因此转化池中可以发生复分解反应生成K4Fe(CN)6,故答案为:相同温度下
,因此转化池中可以发生复分解反应生成K4Fe(CN)6,故答案为:相同温度下![]() 的溶解度小于
的溶解度小于![]() ;
;
(4)从K4Fe(CN)6溶液中得到K4Fe(CN)6,可以通过过滤、洗涤、干燥获得,故答案为:过滤、洗涤、干燥;
(5)实验室K4Fe(CN)6可用于检验Fe3,检验Fe3+反应的离子方程式为K++[Fe(CN)6]4-+Fe3+=KFe[Fe(CN)6]↓;难溶盐KFe[Fe(CN)6可用于治疗Tl2SO4中毒,离子反应方程式为:KFe[Fe(CN)6](s)+Tl+(aq)=TlFe[Fe(CN)6](s)+K+(aq),故答案为: KFe[Fe(CN)6](s)+Tl+(aq)=TlFe[Fe(CN)6](s)+K+(aq);
(6)由图可知,电子从负极流向正极,则a为负极,b为正极,负极发生氧化反应,正极发生还原反应,阳离子向正极移动。
①b为正极,则K+移向催化剂b,故填b;
②a为负极,发生氧化反应,则催化剂a表面发生反应:Fe(CN)64--e-═Fe(CN)63-,故答案为:Fe(CN)64--e-═Fe(CN)63-。

 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案