��Ŀ����
��2012?����ģ�⣩�л��߷��ӻ��������һ�ֳ��õĹ����߷��Ӳ��ϣ���ṹ��ʽΪ��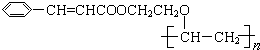 ��
��
��ͼ���Ժϳɼף������Լ��������Է�������Ϊ26������ˮ�ӳ��Ƶã�

��֪��
��-CH2OH+-CH2OH
-CH2OCH2-+H2O
��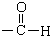 +
+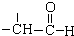
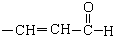 +H2O
+H2O
�ش��������⣺
��1���Լ����������
��2������ͼ��ʾA����Է���������80.5��A��������Ԫ�ص���������Ϊ19.88%��̼Ԫ�ص���������Ϊ29.81%������Ϊ��Ԫ�غ���Ԫ�أ���A�ĺ˴Ź������������������շ壬������ı���Ϊ2��2��1����A�Ľṹ��ʽΪ
��3��д�����з�Ӧ�Ļ�ѧ����ʽ����D��E�ķ�Ӧ +
+
 +NaCl
+NaCl +
+
 +NaCl��
+NaCl��
��4��E��һ��ͬ���칹�壬ˮ����������֣�һ����ʹ��ˮ��ɫ����һ���ڵμӱ�����ˮ���а�ɫ�������ɣ������ʵĽṹ��ʽΪ
 ��
��
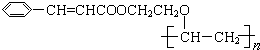 ��
����ͼ���Ժϳɼף������Լ��������Է�������Ϊ26������ˮ�ӳ��Ƶã�

��֪��
��-CH2OH+-CH2OH
| ŨH2SO4 |
| �� |
��
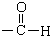 +
+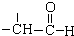
| ||
| �� |
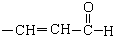 +H2O
+H2O�ش��������⣺
��1���Լ����������
��ȩ
��ȩ
��B��C�ķ�Ӧ��������ȥ��Ӧ
��ȥ��Ӧ
����2������ͼ��ʾA����Է���������80.5��A��������Ԫ�ص���������Ϊ19.88%��̼Ԫ�ص���������Ϊ29.81%������Ϊ��Ԫ�غ���Ԫ�أ���A�ĺ˴Ź������������������շ壬������ı���Ϊ2��2��1����A�Ľṹ��ʽΪ
ClCH2CH2OH
ClCH2CH2OH
����3��д�����з�Ӧ�Ļ�ѧ����ʽ����D��E�ķ�Ӧ
2 +O2
+O2
2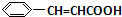 +H2O
+H2O
 +O2
+O2| ���� |
| �� |
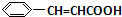 +H2O
+H2O2 +O2
+O2
2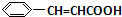 +H2O
+H2O
����C��F�ķ�Ӧ +O2
+O2| ���� |
| �� |
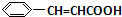 +H2O
+H2O +
+
| һ������ |
 +NaCl
+NaCl +
+
| һ������ |
 +NaCl
+NaCl��4��E��һ��ͬ���칹�壬ˮ����������֣�һ����ʹ��ˮ��ɫ����һ���ڵμӱ�����ˮ���а�ɫ�������ɣ������ʵĽṹ��ʽΪ


������Gͨ���Ӿ۷�Ӧ���ɸ߷��ӻ�����ף��ɼĽṹ��֪��GΪ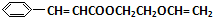 ���Լ��������Է�������Ϊ26������ˮ������Ϊ��Ȳ����Ȳ��ˮ�����ӳɷ�Ӧ������ȩ�����Լ�����CH3CHO������ȩ����ȩ����ϡOH-����������������D���ɷ�Ӧ��Ϣ�ڿ�֪��DΪ
���Լ��������Է�������Ϊ26������ˮ������Ϊ��Ȳ����Ȳ��ˮ�����ӳɷ�Ӧ������ȩ�����Լ�����CH3CHO������ȩ����ȩ����ϡOH-����������������D���ɷ�Ӧ��Ϣ�ڿ�֪��DΪ ��D����������E����EΪ
��D����������E����EΪ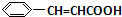 ��E���������Ʒ�Ӧ����F����FΪ
��E���������Ʒ�Ӧ����F����FΪ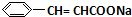 ��F��C��Ӧ����G��NaCl������G�Ľṹ��֪��CΪ
��F��C��Ӧ����G��NaCl������G�Ľṹ��֪��CΪ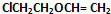 ��A����Է���������80.5��A��������Ԫ�ص���������Ϊ19.88%����ԭ����ĿΪ
��A����Է���������80.5��A��������Ԫ�ص���������Ϊ19.88%����ԭ����ĿΪ
=1��̼Ԫ�ص���������Ϊ29.81%��̼ԭ�ӵ���ĿΪ
=2��̼ԭ������ԭ�ӵ����ԭ������Ϊ12+16=28����A����1��Clԭ�ӣ�A����Hԭ����ĿΪ
=5����A�ķ���ʽΪC2H5OCl��A�ĺ˴Ź������������������շ壬������ı���Ϊ2��2��1����A�Ľṹ��ʽΪClCH2CH2OH���ɷ�Ӧ��Ϣ�ٿ�֪��BΪClCH2CH2OCH2CH2Cl��B���������ƴ���Һ�����������£�����������ȥ��Ӧ����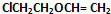 ���ݴ˽��
���ݴ˽��
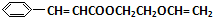 ���Լ��������Է�������Ϊ26������ˮ������Ϊ��Ȳ����Ȳ��ˮ�����ӳɷ�Ӧ������ȩ�����Լ�����CH3CHO������ȩ����ȩ����ϡOH-����������������D���ɷ�Ӧ��Ϣ�ڿ�֪��DΪ
���Լ��������Է�������Ϊ26������ˮ������Ϊ��Ȳ����Ȳ��ˮ�����ӳɷ�Ӧ������ȩ�����Լ�����CH3CHO������ȩ����ȩ����ϡOH-����������������D���ɷ�Ӧ��Ϣ�ڿ�֪��DΪ ��D����������E����EΪ
��D����������E����EΪ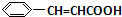 ��E���������Ʒ�Ӧ����F����FΪ
��E���������Ʒ�Ӧ����F����FΪ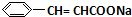 ��F��C��Ӧ����G��NaCl������G�Ľṹ��֪��CΪ
��F��C��Ӧ����G��NaCl������G�Ľṹ��֪��CΪ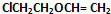 ��A����Է���������80.5��A��������Ԫ�ص���������Ϊ19.88%����ԭ����ĿΪ
��A����Է���������80.5��A��������Ԫ�ص���������Ϊ19.88%����ԭ����ĿΪ| 80.5��19.88% |
| 16 |
| 80.5��29.81% |
| 12 |
| 80.5-35.5-16-12��2 |
| 1 |
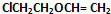 ���ݴ˽��
���ݴ˽������⣺Gͨ���Ӿ۷�Ӧ���ɸ߷��ӻ�����ף��ɼĽṹ��֪��GΪ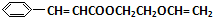 ���Լ��������Է�������Ϊ26������ˮ������Ϊ��Ȳ����Ȳ��ˮ�����ӳɷ�Ӧ������ȩ�����Լ�����CH3CHO������ȩ����ȩ����ϡOH-����������������D���ɷ�Ӧ��Ϣ�ڿ�֪��DΪ
���Լ��������Է�������Ϊ26������ˮ������Ϊ��Ȳ����Ȳ��ˮ�����ӳɷ�Ӧ������ȩ�����Լ�����CH3CHO������ȩ����ȩ����ϡOH-����������������D���ɷ�Ӧ��Ϣ�ڿ�֪��DΪ ��D����������E����EΪ
��D����������E����EΪ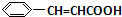 ��E���������Ʒ�Ӧ����F����FΪ
��E���������Ʒ�Ӧ����F����FΪ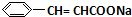 ��F��C��Ӧ����G��NaCl������G�Ľṹ��֪��CΪ
��F��C��Ӧ����G��NaCl������G�Ľṹ��֪��CΪ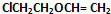 ��A����Է���������80.5��A��������Ԫ�ص���������Ϊ19.88%����ԭ����ĿΪ
��A����Է���������80.5��A��������Ԫ�ص���������Ϊ19.88%����ԭ����ĿΪ
=1��̼Ԫ�ص���������Ϊ29.81%��̼ԭ�ӵ���ĿΪ
=2��̼ԭ������ԭ�ӵ����ԭ������Ϊ12+16=28����A����1��Clԭ�ӣ�A����Hԭ����ĿΪ
=5����A�ķ���ʽΪC2H5OCl��A�ĺ˴Ź������������������շ壬������ı���Ϊ2��2��1����A�Ľṹ��ʽΪClCH2CH2OH���ɷ�Ӧ��Ϣ�ٿ�֪��BΪClCH2CH2OCH2CH2Cl��B���������ƴ���Һ�����������£�����������ȥ��Ӧ����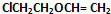 ��
��
��1���Լ��������Է�������Ϊ26������ˮ������Ϊ��Ȳ����Ȳ��ˮ�����ӳɷ�Ӧ������ȩ�����Լ�����CH3CHO��
B��C��ClCH2CH2OCH2CH2Cl�������ƴ���Һ�����������£�����������ȥ��Ӧ����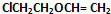 ��
��
�ʴ�Ϊ����ȩ����ȥ��Ӧ��
��2��������������֪��AΪClCH2CH2OH��
�ʴ�Ϊ��ClCH2CH2OH��
��3����D��E�� ����������
����������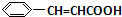 ����Ӧ����ʽΪ��
����Ӧ����ʽΪ��
2 +O2
+O2
2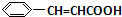 +H2O��
+H2O��
�ʴ�Ϊ��2 +O2
+O2
2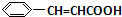 +H2O��
+H2O��
��C��F�ķ�Ӧ��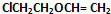 ��
��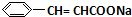 ����
���� ��NaCl����Ӧ����ʽΪ��
��NaCl����Ӧ����ʽΪ�� +
+
 +NaCl��
+NaCl��
�ʴ�Ϊ�� +
+
 +NaCl��
+NaCl��
��4��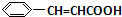 ��һ��ͬ���칹�壬ˮ����������֣�˵�����칹�庬��������һ��ˮ�������ʹ��ˮ��ɫ���ʸ��칹���к���C=C˫������һ��ˮ������ڵμӱ�����ˮ���а�ɫ�������ɣ��ò����к��з��ǻ����ʸ��칹�庬������������ʸ����ʵĽṹ��ʽΪ
��һ��ͬ���칹�壬ˮ����������֣�˵�����칹�庬��������һ��ˮ�������ʹ��ˮ��ɫ���ʸ��칹���к���C=C˫������һ��ˮ������ڵμӱ�����ˮ���а�ɫ�������ɣ��ò����к��з��ǻ����ʸ��칹�庬������������ʸ����ʵĽṹ��ʽΪ ��
��
�ʴ�Ϊ�� ��
��
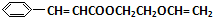 ���Լ��������Է�������Ϊ26������ˮ������Ϊ��Ȳ����Ȳ��ˮ�����ӳɷ�Ӧ������ȩ�����Լ�����CH3CHO������ȩ����ȩ����ϡOH-����������������D���ɷ�Ӧ��Ϣ�ڿ�֪��DΪ
���Լ��������Է�������Ϊ26������ˮ������Ϊ��Ȳ����Ȳ��ˮ�����ӳɷ�Ӧ������ȩ�����Լ�����CH3CHO������ȩ����ȩ����ϡOH-����������������D���ɷ�Ӧ��Ϣ�ڿ�֪��DΪ ��D����������E����EΪ
��D����������E����EΪ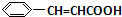 ��E���������Ʒ�Ӧ����F����FΪ
��E���������Ʒ�Ӧ����F����FΪ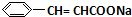 ��F��C��Ӧ����G��NaCl������G�Ľṹ��֪��CΪ
��F��C��Ӧ����G��NaCl������G�Ľṹ��֪��CΪ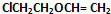 ��A����Է���������80.5��A��������Ԫ�ص���������Ϊ19.88%����ԭ����ĿΪ
��A����Է���������80.5��A��������Ԫ�ص���������Ϊ19.88%����ԭ����ĿΪ| 80.5��19.88% |
| 16 |
| 80.5��29.81% |
| 12 |
| 80.5-35.5-16-12��2 |
| 1 |
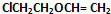 ��
����1���Լ��������Է�������Ϊ26������ˮ������Ϊ��Ȳ����Ȳ��ˮ�����ӳɷ�Ӧ������ȩ�����Լ�����CH3CHO��
B��C��ClCH2CH2OCH2CH2Cl�������ƴ���Һ�����������£�����������ȥ��Ӧ����
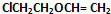 ��
���ʴ�Ϊ����ȩ����ȥ��Ӧ��
��2��������������֪��AΪClCH2CH2OH��
�ʴ�Ϊ��ClCH2CH2OH��
��3����D��E��
 ����������
����������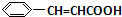 ����Ӧ����ʽΪ��
����Ӧ����ʽΪ��2
 +O2
+O2| ���� |
| �� |
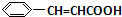 +H2O��
+H2O���ʴ�Ϊ��2
 +O2
+O2| ���� |
| �� |
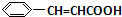 +H2O��
+H2O����C��F�ķ�Ӧ��
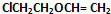 ��
��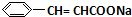 ����
���� ��NaCl����Ӧ����ʽΪ��
��NaCl����Ӧ����ʽΪ�� +
+
| һ������ |
 +NaCl��
+NaCl���ʴ�Ϊ��
 +
+
| һ������ |
 +NaCl��
+NaCl����4��
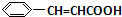 ��һ��ͬ���칹�壬ˮ����������֣�˵�����칹�庬��������һ��ˮ�������ʹ��ˮ��ɫ���ʸ��칹���к���C=C˫������һ��ˮ������ڵμӱ�����ˮ���а�ɫ�������ɣ��ò����к��з��ǻ����ʸ��칹�庬������������ʸ����ʵĽṹ��ʽΪ
��һ��ͬ���칹�壬ˮ����������֣�˵�����칹�庬��������һ��ˮ�������ʹ��ˮ��ɫ���ʸ��칹���к���C=C˫������һ��ˮ������ڵμӱ�����ˮ���а�ɫ�������ɣ��ò����к��з��ǻ����ʸ��칹�庬������������ʸ����ʵĽṹ��ʽΪ ��
���ʴ�Ϊ��
 ��
�����������⿼���л�����ƶϣ��Ƕ��л�֪ʶ���ۺ����ã�ע����ݼĽṹ�ƶ��䵥�壬�ٽ�Ϸ�Ӧ��Ϣ�������������Ʒ�����ƶϣ��ܽϺõĿ��鿼�����Ķ�����ѧ������˼ά�������Ѷ��еȣ����ȵ����ͣ�

��ϰ��ϵ�д�
�����Ŀ