题目内容
科学解释能力是科学素养的重要组成部分。下列对实验现象或操作的解释不合理的是( )
| | 操作及现象 | 解释 |
| A | 在AgI饱和溶液中滴加0.1mol·L—1NaCl溶液,出现白色沉淀 | AgCl的溶解度或Ksp比AgI小,生成更难溶的AgCl沉淀 |
| B | 盛放浓NaOH溶液的试剂瓶用玻璃塞久后,瓶塞很难打开 | NaOH腐蚀玻璃,生成的硅酸钠将瓶口与瓶塞粘在一起 |
| C | 配制FeC13溶液时加入适量盐酸酸化 | 抑制Fe3+水解,防止所配制溶液变浑浊 |
| D | 将氯气通入紫色石蕊溶液中,溶液先变红,后褪色 | 氯气与水反应生成盐酸和次氯酸,溶液显酸性使石蕊溶液变红,次氯酸具有漂白性,使溶液褪色 |
解析试题分析:A、发生沉淀的转化,向溶度积更小的方向移动,AgCl饱和溶液中加入少量NaI溶液产生黄色沉淀,则Ksp(AgI)<Ksp(AgCl);BCD正确。
考点:化学反应实验

练习册系列答案
相关题目
下列装置或操作能达到实验目的的是 ( )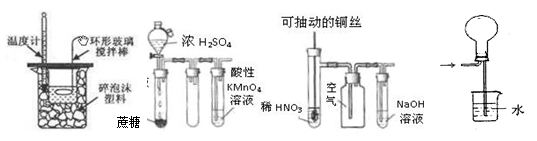
I II III IV
| A.实验I:中和热测定 |
| B.实验II:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 |
| C.实验III:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 |
| D.实验IV:可用于HCl气体的吸收 |
下表各组物质中,不满足如图所示一步转化关系的选项是( )
| 选项 | X | Y | Z |
| A. | Cl2 | NaCl | HCl |
| B. | Fe | FeCl3 | FeCl2 |
| C. | C | CO | CO2 |
| D. | Si | SiO2 | Na2SiO3 |
下列描述中正确的是( )
| A.氯水是纯净物,氯水中的次氯酸具有杀菌消毒作用 |
| B.加碘食盐中所加的“碘”一般是碘化钾 |
| C.氢氧化铁胶体可以使混浊的水变澄清,可作水的消毒剂 |
| D.漂白粉的有效成分是次氯酸钙 |
下列判断错误的是
| A.非金属氧化物不一定是酸性氧化物,金属氧化物不一定为碱性氧化物 |
| B.联合制碱法在滤出NaHCO3后,为使滤液中NH4Cl析出更多更纯,通氨气加食盐冷却 |
| C.发生化学反应时失去电子数越多的金属原子,还原能力不一定越强 |
| D.氯水、Na2O2、活性炭都能使品红溶液褪色,但原理彼此都不相同 |
下列有关几种常见的金属和非金属及其化合物的说法正确的是
| A.铝热反应是指铝能将所有的金属从其氧化物中置换出来 |
| B.Na、Mg、Al、Fe、Cu都能导电,它们的氧化物都能与酸反应 |
| C.CO2、NO、SO2都是非金属氧化物,都属于酸性氧化物 |
D.CaCO3+SiO2 CaSiO3+CO2↑的发生,说明硅酸的酸性强于碳酸 CaSiO3+CO2↑的发生,说明硅酸的酸性强于碳酸 |
下列根据实验操作和现象所得出的结论正确的是:
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 洁净的铁钉在浓硝酸中浸泡片刻,蒸馏水冲洗后,再放入CuSO4溶液 | 铁钉表面无红色物质生成 | 铁钉在浓硝酸中已钝化 |
| B | 向溶液X中先滴加稀NaOH溶液,再将湿润红色石蕊试纸置于试管口附近 | 试纸不变蓝 | 原溶液X中肯定无NH4+ |
| C | 向PbO2中滴入浓盐酸 | 有黄绿色气体 | PbO2具有还原性 |
| D | 向溶液X 中先滴加氯水,再滴加KSCN溶液 | 溶液变红 | 溶液X中一定含有Fe2+ |
下列有关叙述正确的是
| A.Li在空气中燃烧主要生成Li2O2 |
| B.CO2、SO2、NO2都能和碱溶液发生反应, 因此它们都属于酸性氧化物 |
| C.用光束分别照射稀豆浆、硅酸胶体、氢氧化铁胶体,都可以观察到丁达尔效应 |
| D.二氧化硅既能与NaOH反应,又能与HF反应,因此属于两性氧化物 |
