ЬтФПФкШн
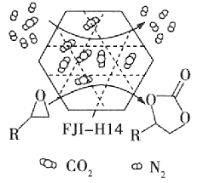
ЁОЬтФПЁПЙ§бѕЛЏИЦ![]() ФбШмгкЫЎЃЌдкГЃЮТЯТЮШЖЈЃЌдкГБЪЊПеЦјМАЫЎжаЛКТ§ЗжНтЗХГібѕЦјЃЌвђЖјЙуЗКгІгУгкгцвЕЁЂХЉвЕЁЂЛЗБЃЕШаэЖрЗНУцЁЃЯТЭМЪЧвдДѓРэЪЏ
ФбШмгкЫЎЃЌдкГЃЮТЯТЮШЖЈЃЌдкГБЪЊПеЦјМАЫЎжаЛКТ§ЗжНтЗХГібѕЦјЃЌвђЖјЙуЗКгІгУгкгцвЕЁЂХЉвЕЁЂЛЗБЃЕШаэЖрЗНУцЁЃЯТЭМЪЧвдДѓРэЪЏ![]() жївЊдгжЪЪЧбѕЛЏЬњ
жївЊдгжЪЪЧбѕЛЏЬњ![]() ЕШЮЊдСЯжЦШЁЙ§бѕЛЏИЦ
ЕШЮЊдСЯжЦШЁЙ§бѕЛЏИЦ![]() ЕФСїГЬЁЃ
ЕФСїГЬЁЃ
ЧыЛиД№ЯТСаЮЪЬтЃК
![]() Вйзї
Вйзї![]() гІАќРЈЯТСаВйзїжаЕФ________ЁЃ
гІАќРЈЯТСаВйзїжаЕФ________ЁЃ![]() ЬюађКХ
ЬюађКХ![]()
A ШмНт ![]() Й§ТЫ
Й§ТЫ ![]() еєСѓ
еєСѓ ![]() ЗжвК
ЗжвК ![]() еєЗЂНсОЇ
еєЗЂНсОЇ
![]() гУАБЫЎЕїНкpHжС
гУАБЫЎЕїНкpHжС![]() ЕФФПЕФЪЧ________ЁЃ
ЕФФПЕФЪЧ________ЁЃ
![]() ШєВтЕУТЫвКCжа
ШєВтЕУТЫвКCжа![]() ЃЌдђ
ЃЌдђ![]() ________
________![]() ЬюЁАЪЧЁБЛђЁАВЛЁБ
ЬюЁАЪЧЁБЛђЁАВЛЁБ![]() ГСЕэЭъШЋЁЃ
ГСЕэЭъШЋЁЃ![]() вбжЊ
вбжЊ![]() ЪБМДПЩЪгЮЊГСЕэЭъШЋЃЛ
ЪБМДПЩЪгЮЊГСЕэЭъШЋЃЛ![]()
![]() ШєдкТЫвКCжаЃЌМгШы
ШєдкТЫвКCжаЃЌМгШы![]() ЪЙШмвКГЪЫсадвдЕУЕНИБВњЮя
ЪЙШмвКГЪЫсадвдЕУЕНИБВњЮя![]() ЃЌдђЫсЛЏКѓШмвКжа
ЃЌдђЫсЛЏКѓШмвКжа![]() ____________
____________![]() ЬюЁА
ЬюЁА![]() ЁБЁЂЁА
ЁБЁЂЁА![]() ЁБЁЂЁА
ЁБЁЂЁА![]() ЁБЁЂЁА
ЁБЁЂЁА![]() ЁБЛђЁА
ЁБЛђЁА![]() ЁБ
ЁБ![]() ЁЃ
ЁЃ
![]() Вйзї
Вйзї![]() ЪЧЃКдкЕЭЮТЯТЃЌЭљЙ§бѕЛЏЧтХЈШмвКжаЭЖШыЮоЫЎТШЛЏИЦНјааЗДгІЃЌвЛЖЮЪБМфКѓЃЌдйМгШыЧтбѕЛЏФЦШмвКЃЌЕБЕїНкШмвКpHжС
ЪЧЃКдкЕЭЮТЯТЃЌЭљЙ§бѕЛЏЧтХЈШмвКжаЭЖШыЮоЫЎТШЛЏИЦНјааЗДгІЃЌвЛЖЮЪБМфКѓЃЌдйМгШыЧтбѕЛЏФЦШмвКЃЌЕБЕїНкШмвКpHжС![]() ЃЌВХГіЯжДѓСПГСЕэЁЃаДГіИУЗДгІЕФЛЏбЇЗНГЬЪН________ЃЛгУМђвЊЕФЮФзжНтЪЭгУЧтбѕЛЏФЦЕїНкpHжС
ЃЌВХГіЯжДѓСПГСЕэЁЃаДГіИУЗДгІЕФЛЏбЇЗНГЬЪН________ЃЛгУМђвЊЕФЮФзжНтЪЭгУЧтбѕЛЏФЦЕїНкpHжС![]() ЕФдвђ_________ЁЃ
ЕФдвђ_________ЁЃ
![]() вбжЊДѓРэЪЏКЌ
вбжЊДѓРэЪЏКЌ![]() ЕФжЪСПЗжЪ§ЮЊaЃЌ
ЕФжЪСПЗжЪ§ЮЊaЃЌ![]() ДѓРэЪЏПЩвджЦЕУ
ДѓРэЪЏПЩвджЦЕУ![]() ЃЌЧыМЦЫуЃК
ЃЌЧыМЦЫуЃК![]() зЊЛЏЮЊ
зЊЛЏЮЊ![]() Й§ГЬжаЃЌCaдзгЕФРћгУТЪ________ЁЃ
Й§ГЬжаЃЌCaдзгЕФРћгУТЪ________ЁЃ
ЁОД№АИЁП![]() Г§ШЅ
Г§ШЅ![]() ЪЧ
ЪЧ ![]()
![]() Лђ
Лђ![]() МгШыNaOHШмвКЪЙЩЯЪіЦНКтЯђе§ЗДгІЗНЯђвЦЖЏЃЌгаРћгк
МгШыNaOHШмвКЪЙЩЯЪіЦНКтЯђе§ЗДгІЗНЯђвЦЖЏЃЌгаРћгк![]() ГСЕэЕФЩњГЩ
ГСЕэЕФЩњГЩ ![]()
ЁОНтЮіЁП
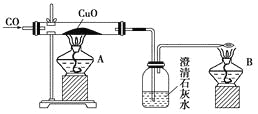
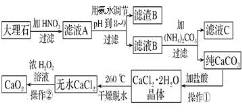
ИљОнЭМЪОаХЯЂЃЌПЩЕУГіЃКТЫвКAЕФГЩЗжгаЯѕЫсИЦКЭЯѕЫсЬњвдМАЪЃгрЕФЯѕЫсЃЌЕБpHжС8-9ЗЖЮЇЖЮФкЪБЃЌШ§МлЬњПЩвзаЮГЩГСЕэЃЌЫљвдТЫдќBЪЧЧтбѕЛЏЬњЃЌТЫвКBЪЧЯѕЫсИЦЃЌКЭЬМЫсяЇжЎМфПЩвдЗЂЩњИДЗжНтЗДгІЩњГЩЬМЫсИЦКЭЯѕЫсяЇЃЌЙ§ТЫЃЌГСЕэЬМЫсИЦгУбЮЫсШмНтШЛКѓеєЗЂНсОЇПЩвдЕУЕНТШЛЏИЦОЇЬхЃЌдйЪЇЫЎГЩЮЊЮоЫЎТШЛЏИЦЃЌЫЋбѕЫЎПЩвдКЭТШЛЏИЦЗДгІЩњГЩЙ§бѕЛЏИЦКЭбЮЫсЁЃ
ЃЈ1ЃЉЯђДПЬМЫсИЦжаМгбЮЫсЃЌНЋЙЬЬхШмНтЃЌШЛКѓеєЗЂХЈЫѕЁЂРфШДНсОЇЁЂЙ§ТЫПЩЕУCaCl2.2H2OЃЌЙЪАќРЈABEЃЛ
ЃЈ2ЃЉЯђДѓРэЪЏ(жївЊдгжЪЪЧбѕЛЏЬњ)жаМгШыЯѕЫсЃЌТЫвКAжаКЌдгжЪFe3+ЃЌМгШыАБЫЎНЋFe3+зЊЛЏЮЊFe(OH)3ЖјГ§ШЅЃЛ
ЃЈ3ЃЉc(Ca2ЃЋ)=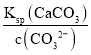 =
=![]() ЃМ10Ѓ5mol/LЃЌдђCa2ЃЋвбГСЕэЭъШЋЃЛ
ЃМ10Ѓ5mol/LЃЌдђCa2ЃЋвбГСЕэЭъШЋЃЛ
ЃЈ4ЃЉNH4NO3ШмвКжаЃЌNH4+ЫЎНтШмвКЯдЫсадЃЌЫљвдc(NH![]() )ЃМc(NO
)ЃМc(NO![]() )ЃЛ
)ЃЛ
ЃЈ5ЃЉгЩЬтвтПЩжЊЃЌЛЏбЇЗНГЬЪНЮЊCaCl2ЃЋH2O2![]() CaO2ЃЋ2HCl(ЛђCaCl2ЃЋH2O2ЃЋ2NaOH=CaO2Ё§ЃЋ2NaClЃЋ2H2O)ЃЛгУЧтбѕЛЏФЦЕїНкpHжС9ЁЋ11ЕФдвђЪЧЃКCaCl2ЃЋH2O2
CaO2ЃЋ2HCl(ЛђCaCl2ЃЋH2O2ЃЋ2NaOH=CaO2Ё§ЃЋ2NaClЃЋ2H2O)ЃЛгУЧтбѕЛЏФЦЕїНкpHжС9ЁЋ11ЕФдвђЪЧЃКCaCl2ЃЋH2O2![]() CaO2ЃЋ2HClЃЌМгШыNaOHШмвКЪЙЩЯЪіЦНКтЯђе§ЗДгІЗНЯђвЦЖЏЃЌгаРћгкCaO2ГСЕэЕФЩњГЩЃЛ
CaO2ЃЋ2HClЃЌМгШыNaOHШмвКЪЙЩЯЪіЦНКтЯђе§ЗДгІЗНЯђвЦЖЏЃЌгаРћгкCaO2ГСЕэЕФЩњГЩЃЛ
ЃЈ6ЃЉИљОнИЦЪиКуПЩЕУЙиЯЕЪНЃЌCaCO3~CaO2ЃЌдђCaдзгЕФРћгУТЪЮЊЃК![]() =
=![]() ЁЃ
ЁЃ

ЁОЬтФПЁПКЌЕЊЛЏКЯЮядкЩњВњЁЂЩњУќЛюЖЏжагаживЊЕФзїгУЁЃЛиД№ЯТСаЮЪЬтЃК
(1)вбжЊ4NH3(g)+5O2(g)=4NO(g)+6H2O(g)ЁїH1=ЃalkJ/molЃЌ4NH3(g)+6NO(g)=5N2(g)+6H2O(g)ЁїH2=ЃbkJ/molЃЌH2O(1)=H2O(g)ЁїH3=+ckJ/molЃЌаДГідк298KЪБЃЌАБЦјШМЩеЩњГЩN2ЕФШШЛЏбЇЗНГЬЪН___________ЁЃ
(2)МЁШтжаЕФМЁКьЕААз(Mb)ПЩгыO2НсКЯЩњГЩMbO2ЃКMb(aq)+O2(g)![]() MbO2(aq)ЃЌЦфжаkе§КЭkФцЗжБ№БэЪОе§ЗДгІКЭФцЗДгІЕФЫйТЪГЃЪ§ЃЌМДVе§=kе§ЁЄc(Mb)ЁЄP(O2)ЃЌVФц=kФцЁЄc(MbO2)ЁЃ37ЁцЪБВтЕУМЁКьЕААзЕФНсКЯЖШ(ІС)гыP(O2)ЕФЙиЯЕШчЯТБэ[НсКЯЖШ(ІС)жИвбгыO2НсКЯЕФМЁКьЕААзеМзмМЁКьЕААзЕФАйЗжБШ]ЃК
MbO2(aq)ЃЌЦфжаkе§КЭkФцЗжБ№БэЪОе§ЗДгІКЭФцЗДгІЕФЫйТЪГЃЪ§ЃЌМДVе§=kе§ЁЄc(Mb)ЁЄP(O2)ЃЌVФц=kФцЁЄc(MbO2)ЁЃ37ЁцЪБВтЕУМЁКьЕААзЕФНсКЯЖШ(ІС)гыP(O2)ЕФЙиЯЕШчЯТБэ[НсКЯЖШ(ІС)жИвбгыO2НсКЯЕФМЁКьЕААзеМзмМЁКьЕААзЕФАйЗжБШ]ЃК
P(O2) | 0.50 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 | 6.00 |
ІСЃЈMbO2%ЃЉ | 50.0 | 67.0 | 80.0 | 85.0 | 88.0 | 90.3 | 91.0 |
ЂйМЦЫу37ЁцЁЂP(O2)ЮЊ2.00kPaЪБЃЌЩЯЪіЗДгІЕФЦНКтГЃЪ§K=___________ЁЃ
ЂкЕМГіЦНКтЪБМЁКьЕААзгыO2ЕФНсКЯЖШ(ІС)гыO2ЕФбЙЧП[P(O2)]жЎМфЕФЙиЯЕЪНІС=___________(гУКЌгаkе§ЁЂkФцЕФЪНзгБэЪО)ЁЃ
(3)ЙЙГЩМЁКьЕААзЕФИЪАБЫс(NH2CH2COOH)ЪЧвЛжжСНадЮяжЪЃЌдкШмвКжавдШ§жжРызгаЮЪНДцдкЃЌЦфзЊЛЏЙиЯЕШчЯТЃК
![]()
![]()
![]()
![]()
![]()
дкИЪАБЫсШмвКжаМгШыЫсЛђМюЃЌШ§жжРызгЕФАйЗжКЌСПгы![]() ЕФЙиЯЕШчЭМЫљЪОЃК
ЕФЙиЯЕШчЭМЫљЪОЃК

ЂйДПИЪАБЫсШмвКГЪ___________адЃЛЕБШмвКГЪжаадЪБШ§жжРызгЕФХЈЖШгЩДѓЕНаЁЕФЫГађЮЊ___________ЁЃ
ЂкЯђ![]() =8ЕФШмвКжаМгШыЙ§СПHClЪБЃЌЗДгІЕФРызгЗНГЬЪНЮЊ___________ЁЃ
=8ЕФШмвКжаМгШыЙ§СПHClЪБЃЌЗДгІЕФРызгЗНГЬЪНЮЊ___________ЁЃ
ЂлгУЕчЮЛЕЮЖЈЗЈПЩВтЖЈФГИЪАБЫсбљЦЗЕФДПЖШ.

ГЦШЁбљЦЗ150mgЃЌдквЛЖЈЬѕМўЯТЃЌгУ0.1000mol/LЕФИпТШЫсШмвКЕЮЖЈ(гыИЪАБЫс1ЉU1ЗЂЩњЗДгІ)ЃЌВтЕУЕчбЙБфЛЏгыЕЮШыHClO4ШмвКЕФЬхЛ§ЙиЯЕШчЯТЭМЁЃзіПеАзЖдееЪЕбщЃЌЯћКФHClO4ШмвКЕФЬхЛ§ЮЊ0.25mLЃЌИУбљЦЗЕФДПЖШЮЊ___________%(МЦЫуНсЙћБЃСєвЛЮЛаЁЪ§)