题目内容
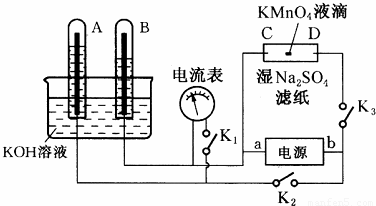
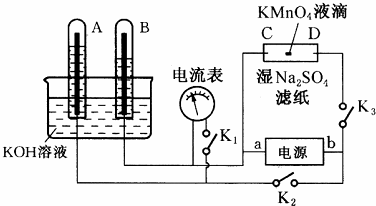
如图装置,A、B中的电极为多孔的惰性电极;C、D为夹在湿的Na2SO4滤纸条上的铂夹;电源有a、b两极.若A、B中充满KOH溶液后倒立于KOH溶液的水槽中.切断K1,合闭K2、K3通直流电,回答下列问题:
①判断电源的正、负极:a为
②在湿的Na2SO4溶液滤纸条中心的KMnO4液滴,有什么现象
③写出电极反应式:A极
④若电解一段时间后,A、B中均有气体包围电极.此时切断K2、K3,合闭K1,则电流表的指针是否移动(填是或否)

①判断电源的正、负极:a为
负、
负、
极,b为正
正
极.②在湿的Na2SO4溶液滤纸条中心的KMnO4液滴,有什么现象
紫色向D方向移动,两极有气体产生
紫色向D方向移动,两极有气体产生
.③写出电极反应式:A极
4OH--4e=2H2O+O2↑,
4OH--4e=2H2O+O2↑,
,C极4H++4e=2H2↑.
4H++4e=2H2↑.
.④若电解一段时间后,A、B中均有气体包围电极.此时切断K2、K3,合闭K1,则电流表的指针是否移动(填是或否)
是
是
.说明理由组成氢氧燃料电池
组成氢氧燃料电池
.分析:①根据A、B两电极得到的气体体积判断电极名称,从而确定电源a、b电极名称;
②先判断C、D 的电极名称,判断电解时溶液中离子的移动方向;
③根据离子的放电顺序书写电极反应式;
④根据原电池的构成条件判断.
②先判断C、D 的电极名称,判断电解时溶液中离子的移动方向;
③根据离子的放电顺序书写电极反应式;
④根据原电池的构成条件判断.
解答:解:①切断K1,合闭K2、K3通直流电,电极A、B及氢氧化钾溶液构成电解池,根据离子的放电顺序,溶液中氢离子、氢氧根离子放电,分别生成氢气和氧气,氢气和氧气的体积比为2:1,通过图象知,B极上气体体积是A极上气体体积的2倍,所以B极上得氢气,A极上得到氧气,所以B极是阴极,A极是阳极,故a是负极,b是正极.
故答案为:负;正;
②浸有硫酸钠的滤纸和电极C、D与电源也构成了电解池,因为a是负极,b是正极,所以C是阴极,D是阳极,电解质溶液中的阳离子钾离子向阴极移动,阴离子高锰酸根离子向阳极移动,所以D极呈紫色;电解质溶液中氢离子和氢氧根离子放电,所以在两极上都得到气体.
故答案为:紫色向D方向移动,两极有气体产生;
③A极上氢氧根离子失电子生成氧气和水,电极反应式为4OH--4e=2H2O+O2↑;C极上氢离子得电子生成氢气,电极反应式为4H++4e=2H2↑.
故答案为:4OH--4e=2H2O+O2↑;4H++4e=2H2↑;
④切断K2、K3,合闭K1,电解一段时间后,A、B中均有气体包围电极.此装置构成氢氧燃料原电池,所以有电流通过,电流表的指针移动.
故答案为:是;组成氢氧燃料电池.
故答案为:负;正;
②浸有硫酸钠的滤纸和电极C、D与电源也构成了电解池,因为a是负极,b是正极,所以C是阴极,D是阳极,电解质溶液中的阳离子钾离子向阴极移动,阴离子高锰酸根离子向阳极移动,所以D极呈紫色;电解质溶液中氢离子和氢氧根离子放电,所以在两极上都得到气体.
故答案为:紫色向D方向移动,两极有气体产生;
③A极上氢氧根离子失电子生成氧气和水,电极反应式为4OH--4e=2H2O+O2↑;C极上氢离子得电子生成氢气,电极反应式为4H++4e=2H2↑.
故答案为:4OH--4e=2H2O+O2↑;4H++4e=2H2↑;
④切断K2、K3,合闭K1,电解一段时间后,A、B中均有气体包围电极.此装置构成氢氧燃料原电池,所以有电流通过,电流表的指针移动.
故答案为:是;组成氢氧燃料电池.
点评:本题考查了原电池、电解池工作原理,写电极反应式要注意结合电解质溶液书写,如果电解质溶液不同,虽然原料相同,电极反应式也不同,如氢氧燃料电池,当电解质为酸或碱,电极反应式就不同.

练习册系列答案
相关题目