题目内容
【题目】自然界中含锰元素的主要矿物有软锰矿(MnO2·xH2O)、黑锰矿Mn3O4,大洋底部有大量锰结核矿。锰元素在多个领域中均有重要应用,用于制合金,能改善钢的抗冲击性能等。
(1)Mn在元素周期表中位于___区,核外电子占据最高能层的符号是___,金属锰可导电,导热,具有金属光泽,有延展性,这些性质都可以用“___理论”解释。
(2)Mn3+在水溶液中容易歧化为MnO2和Mn2+,下列说法合理的是___。
A.Mn3+的价电子构型为3d4,不属于较稳定的电子构型
B.根据Mn2+的电子构型可知,Mn2+中不含成对电子
C.第四周期元素中,锰原子价电子层中未成对电子数最多
D.Mn2+与Fe3+具有相同的价电子构型,所以它们的化学性质相似
(3)在K2MnF6中,MnF62-的空间构型是正八面体,则中心原子的价层电子对数为__。该化合物中含有的共价键在形成过程中原子轨道的重叠方式为__。
(4)二价锰的化合物MnO和MnS熔融态均能导电,熔点MnO___MnS(选填“高于”、“等于”、“低于”)并解释原因___。
(5)某锰氧化物的晶胞结构如图:
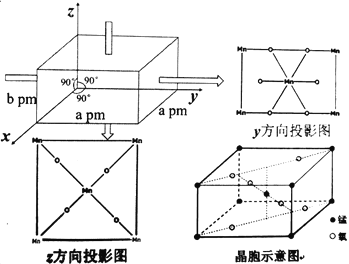
该锰的氧化物的化学式为___,该晶体中Mn的配位数为____,该晶体中Mn之间的最近距离为___pm(用a、b来表示)。
【答案】d N 电子气 A 6 “头碰头” 高于 均为离子晶体,O2-半径比S2-半径小,MnO晶格能大,熔点高 MnO2 6 ![]()
【解析】
(1)Mn是25号元素,原子核外电子排布式是1s22s22p63s23p63d54s2;锰可导电,导热,具有金属光泽,有延展性,是因为有自由电子,这些性质都可以用“电子气理论”解释;
(2)A.Mn3+在水溶液中容易歧化为MnO2和Mn2+,说明Mn3+不稳定;
B.Mn2+中价电子层不含成对电子,但是内层中含有成对电子;
C.第四周期中价电子层中未成对电子数最多的元素价电子排布式为:3d54s1;
D.Mn2+与Fe3+具有相同的价电子构型,微粒的化学性质不仅与价电子构型有关,也和微粒的电荷数、微粒半径、原子序数有关;
(3)MnF62的空间构型是正八面体,则中心原子的价层电子对数为6;F与Mn之间的共价键都是共价单键;
(4)物质都属于离子晶体,离子晶体的阴离子带有相同电荷,离子半径越小,离子键越强,晶格能越大,熔点越高;
(5)用均摊法计算确定化学式,并结合微粒的空间排列确定Mn的配位数;由晶胞结构可知:在该晶胞中距离相等且最近的2个Mn在晶胞体对角线的一半。
(1)Mn是25号元素,原子核外电子排布式是1s22s22p63s23p63d54s2,可知M在元素周期表中位于第四周期第VIIB,属于d区元素,核外电子占据最高能层的符号是N;锰可导电,导热,具有金属光泽,有延展性,是因为有自由电子,这些性质都可以用“电子气理论”解释,故答案为:d;N;电子气;
(2)A.Mn3+的价电子构型为3d4,Mn3+在水溶液中容易歧化为MnO2和Mn2+,说明Mn3+不稳定,Mn3+容易变成电子半充满的稳定的价电子构型为3d5,3d4则属于不稳定的电子构型,故A正确;
B.Mn2+中价电子层不含成对电子,但是内层中含有成对电子,故B错误;
C.第四周期中价电子层中未成对电子数最多的元素价电子排布式为:3d54s1,是Cr元素,故C错误;
D.Mn2+与Fe3+具有相同的价电子构型,微粒的化学性质不仅与价电子构型有关,也和微粒的电荷数、微粒半径、原子序数有关,因此它们的化学性质不相似,Mn2+具有强的还原性,而Fe3+具有强的氧化性,故D错误;
故答案选:A;
(3)MnF62的空间构型是正八面体,则中心原子的价层电子对数为6.在化合物化合物K2MnF6中含有的F与Mn之间的共价键都是共价单键,属于σ键,在形成过程中原子轨道的重叠方式为“头碰头”,故答案为:6;“头碰头”;
(4)MnO和MnS都是离子晶体,离子电荷数相同,O2离子半径小于S2的离子半径,MnO的晶格能大,熔点更高,故答案为:高于;均为离子晶体,O2-半径比S2-半径小,MnO晶格能大,熔点高;
(5)在该晶体中含有的Mn原子个数为:![]() ×8+1=2,含有的O原子数目为:
×8+1=2,含有的O原子数目为:![]() ×4+2=4,Mn:O=2:4=1:2,所以该锰的氧化物的化学式为MnO2;根据晶胞投影图可知:在该晶体体中与Mn原子距离相等且最近的O原子有6个,所以Mn的配位数为6;由晶胞结构可知:在该晶胞中距离相等且最近的2个Mn在晶胞体对角线的一半,晶胞的体对角线为
×4+2=4,Mn:O=2:4=1:2,所以该锰的氧化物的化学式为MnO2;根据晶胞投影图可知:在该晶体体中与Mn原子距离相等且最近的O原子有6个,所以Mn的配位数为6;由晶胞结构可知:在该晶胞中距离相等且最近的2个Mn在晶胞体对角线的一半,晶胞的体对角线为![]() pm,所以该晶体中Mn之间的最近距离为
pm,所以该晶体中Mn之间的最近距离为![]() ×
×![]() pm=
pm=![]() pm,故答案为:MnO2;6;
pm,故答案为:MnO2;6;![]() 。
。

【题目】氨气常用作合成氯氨类化合物,是常用的饮用水二级消毒剂,主要包括一氯胺、二氯胺和三氯胺(NH2C1、NHCl2和NCl3),副产物少于其它水消毒剂。
回答下列问题:
(1)工业上可利用反应Cl2(g)+NH3(g)=NH2Cl(l)+HCl(g)制备一氯胺,已知部分化学键的键能如下表所示(假设不同物质中同种化学键的键能相同),则该反应的△H=___kJ/mol。
化学键 | N-H | Cl-Cl | N-Cl | H-Cl |
键能(kJ/mol) | 391.3 | 243.0 | 191.2 | 431.8 |
一氯胺是重要的水消毒剂,其原因是由于一氯胺在中性、酸性环境中会发生完全水解,生成具有强烈杀菌消毒作用的物质,该水解反应的化学方程式为___。
(2)用Cl2和NH3反应制备二氯胺的方程式为2Cl2(g)+NH3(g)![]() NHCl2(g)+2HCl(g)。在恒温条件下,3molCl2和1molNH3发生反应,测得平衡时Cl2和HCl的物质的量浓度与平衡总压的关系如图所示:
NHCl2(g)+2HCl(g)。在恒温条件下,3molCl2和1molNH3发生反应,测得平衡时Cl2和HCl的物质的量浓度与平衡总压的关系如图所示:
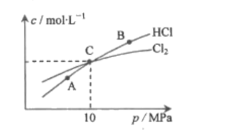
①A、B、C三点中Cl2转化率最高的是___点(填“A”“B”或“C")。
②计算C点时该反应的压强平衡常数Kp(C)=____(Kp是平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(3)我国研制出非贵金属镍钼基高效电催化剂,实现电解富尿素废水低能耗制H2(装置如图),总反应为:CO(NH2)2+H2O![]() 3H2↑+N2↑+CO2↑。
3H2↑+N2↑+CO2↑。
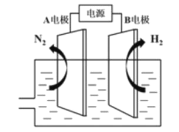
①A电极连接电源的___极(填"正”或“负”)。
②A电极的电极反应为___。