题目内容
标准状态下质量比为14:15的N2和NO气体,N2和NO的物质的量之比为________,密度之比为________如将其混合氮原子和氧原子的个数比为________.
1:1 14:15 3:1
分析:利用n= 来计算物质的量,利用构成计算原子的个数比,由pM=ρRT可知,标准状态下气体的密度之比等于摩尔质量之比.
来计算物质的量,利用构成计算原子的个数比,由pM=ρRT可知,标准状态下气体的密度之比等于摩尔质量之比.
解答:由质量比为14:15的N2和NO气体,
设N2和NO的质量分别为14g、15g,则
N2和NO的物质的量之比为 :
: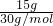 =1:1,
=1:1,
由pM=ρRT可知,标准状态下气体的密度之比等于摩尔质量之比,
则密度之比等于28g/mol:30g/mol=14:15,
将物质的量之比为1:1的气体混合,
氮原子和氧原子的个数比为(1×2+1):1=3:1,
故答案为:1:1;14:15;3:1.
点评:本题考查物质的量的计算,明确常见物质的摩尔质量及质量与物质的量的关系、分子的构成、阿伏伽德罗定律的推论等即可解答.
分析:利用n=
 来计算物质的量,利用构成计算原子的个数比,由pM=ρRT可知,标准状态下气体的密度之比等于摩尔质量之比.
来计算物质的量,利用构成计算原子的个数比,由pM=ρRT可知,标准状态下气体的密度之比等于摩尔质量之比.解答:由质量比为14:15的N2和NO气体,
设N2和NO的质量分别为14g、15g,则
N2和NO的物质的量之比为
 :
: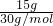 =1:1,
=1:1,由pM=ρRT可知,标准状态下气体的密度之比等于摩尔质量之比,
则密度之比等于28g/mol:30g/mol=14:15,
将物质的量之比为1:1的气体混合,
氮原子和氧原子的个数比为(1×2+1):1=3:1,
故答案为:1:1;14:15;3:1.
点评:本题考查物质的量的计算,明确常见物质的摩尔质量及质量与物质的量的关系、分子的构成、阿伏伽德罗定律的推论等即可解答.

练习册系列答案
相关题目
 某种含有少量氧化钠的过氧化钠试样质量为1.56g,为测定各成分的质量分数,按如图所示,原锥形瓶和水的总质量为190.72,将1.56g上述样品投入锥形瓶中,充分反应后,电子天平最终的读数为192.12g.
某种含有少量氧化钠的过氧化钠试样质量为1.56g,为测定各成分的质量分数,按如图所示,原锥形瓶和水的总质量为190.72,将1.56g上述样品投入锥形瓶中,充分反应后,电子天平最终的读数为192.12g. 某种含有少量氧化钠的过氧化钠试样质量为1.56g,为测定各成分的质量分数,按如图所示,原锥形瓶和水的总质量为190.72,将1.56g上述样品投入锥形瓶中,充分反应后,电子天平最终的读数为192.12g.
某种含有少量氧化钠的过氧化钠试样质量为1.56g,为测定各成分的质量分数,按如图所示,原锥形瓶和水的总质量为190.72,将1.56g上述样品投入锥形瓶中,充分反应后,电子天平最终的读数为192.12g.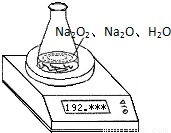
 mol氢原子,其质量为______________,在标准状态下的体积为______________。
mol氢原子,其质量为______________,在标准状态下的体积为______________。