��Ŀ����
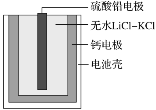
����Ŀ���ȼ����ؿ���������������Ĺ�����Դ��һ���ȼ����صĻ����ṹ��ͼ��ʾ��������Ϊ����ʵ���ˮLiCl��KCl������������ں�ؼ���˲��������ܡ��õ���ܷ�ӦΪPbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb�������й�˵����ȷ����
A.�ŵ�����У�Cl-�������ƶ�
B.������Ӧʽ��PbSO4+2e��=Pb+SO42��
C.��Ӧÿת��0.1mol���ӣ���������������4g Ca
D.����ʱ��������������ϵ�������ָ�뷢��ƫת
���𰸡�B
��������
��ԭ����ܷ�Ӧ��֪CaΪԭ��صĸ���������������Ӧ�ĵ缫����ʽΪCa-2e-=Ca2+��PbSO4Ϊԭ��ص�������������ԭ��Ӧ���缫����ʽΪPbSO4+2e-=SO42-+Pb��ԭ��ع���ʱ���������������ƶ������������ƶ�����ϵ�ⷽ��ʽ���㡣
A���ŵ����Ϊԭ��أ����������ƶ���Cl-���ƶ�����A����
B������������ԭ��Ӧ��������Ӧʽ��PbSO4+2e��=Pb+SO42������B��ȷ��
C��CaΪԭ��صĸ����������������ݵ缫����ʽCa+2Cl--2e-=CaCl2����Ӧÿת��0.1mol���ӣ���������������0.05molCa������m=nM=0.05mol��40g/mol=2g����C����
D�������£�����ʲ�������̬�����Ӳ����ƶ������ܲ���������������ӵ�����������ƣ�ָ�벻ƫת����D����
��ѡB��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ��T��ʱ����A��B��0.32mol��������ܱ������У�������Ӧ��A(g)��B(g)![]() 2C(g)��H=-akJ��mol-1(a>0)����Ӧ�����вⶨ���������±�������˵����ȷ���ǣ� ��
2C(g)��H=-akJ��mol-1(a>0)����Ӧ�����вⶨ���������±�������˵����ȷ���ǣ� ��
t/min | 0 | 2 | 4 | 7 | 9 |
n(B)/mol | 0.32 | 0.24 | 0.22 | 0.20 | 0.20 |
A.����ʼʱ�������г���0.64molC�����ƽ��ʱ���յ�����Ϊ0.12akJ
B.���£����ѹ�����������B��Ũ�Ⱥ��������������
C.����ʼʱ�������г���0.64molA��0.64molB�����ƽ��ʱn(C)<0.40mol
D.���¡����ݣ���ƽ����ϵ���ٳ���0.32molA���ٴ�ƽ��ʱ��B��ת��������