题目内容
“绿色化学”是21世纪化学发展的主导方向。“绿色化学”要求从根本上消灭污染。其中“化学反应的绿色化”要求原料物质中所有的原子完全被利用且全部转入期望的产品中。
(1)下列符合“化学反应的绿色化”的是( )
①用铁屑、氧化铜、稀硫酸为原料制取铜:CuO+H2SO4====CuSO4+H2O,Fe+CuSO4====FeSO4+Cu
②用甲烷、一氧化碳合成乙酸乙酯:2CH4+2CO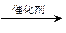 CH3COOC2H5
CH3COOC2H5
③乙烯催化氧化制乙醛:2C2H4+O2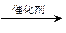 CH3CHO
CH3CHO
④2M+N====2P+2Q,2P+M====Q(M、N为原料,Q为期望产品)
(2)污染气体的几种处理措施:
酸雨是由于大气中SO2和NOx(NO和NO2)的含量不断升高,并转变为H2SO4和HNO3(主要是H2SO4)随雨水降落而形成的。为防止污染,硫酸厂用氨水来吸收SO2,离子方程式为_____________;硝酸厂可用烧碱溶液来吸收氮的氧化物,如NO2被烧碱溶液吸收生成NaNO2和NaNO3,离子方程式为________________;也可用氨的催化还原法把氮的氧化物变成氮气,还原1体积的NOx需要____________体积氨气。
(1)下列符合“化学反应的绿色化”的是( )
①用铁屑、氧化铜、稀硫酸为原料制取铜:CuO+H2SO4====CuSO4+H2O,Fe+CuSO4====FeSO4+Cu
②用甲烷、一氧化碳合成乙酸乙酯:2CH4+2CO
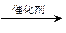 CH3COOC2H5
CH3COOC2H5③乙烯催化氧化制乙醛:2C2H4+O2
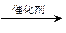 CH3CHO
CH3CHO④2M+N====2P+2Q,2P+M====Q(M、N为原料,Q为期望产品)
| A.②③④ | B.①②④ | C.①③④ | D.①②③ |
酸雨是由于大气中SO2和NOx(NO和NO2)的含量不断升高,并转变为H2SO4和HNO3(主要是H2SO4)随雨水降落而形成的。为防止污染,硫酸厂用氨水来吸收SO2,离子方程式为_____________;硝酸厂可用烧碱溶液来吸收氮的氧化物,如NO2被烧碱溶液吸收生成NaNO2和NaNO3,离子方程式为________________;也可用氨的催化还原法把氮的氧化物变成氮气,还原1体积的NOx需要____________体积氨气。
(1)B
(2)2NH3·H2O+SO2====2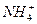 +
+ +H2O
+H2O
2NO2+2OH-====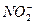 +
+ +H2O
+H2O
2x/3
(2)2NH3·H2O+SO2====2
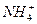 +
+ +H2O
+H2O2NO2+2OH-====
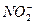 +
+ +H2O
+H2O2x/3
据绿色化学含义只有③的原料的原子没被充分利用,不符合,选B。(2)中据反应物可写出前两问的答案依次为:2NH3·H2O+SO2====2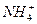 +
+ +H2O。
+H2O。
2NO2+2OH-====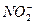 +
+ +H2O。用氨的催化还原的方程式为3NOx+2xNH3====(x+3/2)N2+3xH2O,则每还原1体积的NOx需要2x/3体积的氨气。
+H2O。用氨的催化还原的方程式为3NOx+2xNH3====(x+3/2)N2+3xH2O,则每还原1体积的NOx需要2x/3体积的氨气。
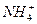 +
+ +H2O。
+H2O。2NO2+2OH-====
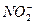 +
+ +H2O。用氨的催化还原的方程式为3NOx+2xNH3====(x+3/2)N2+3xH2O,则每还原1体积的NOx需要2x/3体积的氨气。
+H2O。用氨的催化还原的方程式为3NOx+2xNH3====(x+3/2)N2+3xH2O,则每还原1体积的NOx需要2x/3体积的氨气。
练习册系列答案
相关题目
 N2 + 2CO2将有害的污染物转化为可参与大气循环的N2和CO2。
N2 + 2CO2将有害的污染物转化为可参与大气循环的N2和CO2。
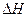 ▲ 0(“>”、“<”、“=”)。
▲ 0(“>”、“<”、“=”)。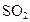 是常见的大气污染物之一,我国规定空气中
是常见的大气污染物之一,我国规定空气中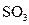 ④使用
④使用 作萃取剂除去煤炭中的硫 ⑤燃烧煤中加入石灰石后使用
作萃取剂除去煤炭中的硫 ⑤燃烧煤中加入石灰石后使用