题目内容
海洋是生命的摇篮、资源的宝库。中国要实施海洋强国战略,实现由海洋大国向海洋强国迈进的梦想。海洋经济已经成为拉动我国国民经济发展的重要引擎,海水的综合开发、利用是海洋经济的一部分,海水中可提取多种化工原料,下面是工业上对海水的几项综合利用的示意图。其流程如下图所示:
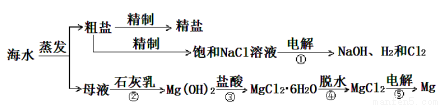
(1)写出①、②反应的离子方程式:
①______________________,②______________________。
(2)工业上利用电解饱和食盐水产生的氢气和氯气制取盐酸,为了体现绿色化学理念,使氯气充分反应,采取将氯气在氢气中燃烧的办法,可避免氯气燃烧不完全污染空气,请写出氯气在氢气中燃烧的实验现象:______________________。
(3)粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制后可得到饱和NaC1溶液。现有下列除杂试剂:A.盐酸 B.氢氧化钡溶液 C.碳酸钠溶液。精制时加入过量除杂试剂的正确顺序是______________。(填序号)
(4)金属镁在空气中燃烧时,除生成MgO外,还有少量Mg3N2生成。把等物质的量的金属镁分别放在:A.纯氧气(O2)中;B.二氧化碳气体中;C.空气中。完全燃烧后,得到的固体物质的质量由大到小的顺序是______________。(填序号)
(5)将电解饱和NaCl溶液生成的氯气通入氢氧化钠溶液中可以得到NaClO。某化学兴趣小组探究NaClO与尿素CO(NH2)2的反应产物,通过实验发现产物除某种盐外,其余产物都是能参与大气循环的物质,则该反应的化学方程式为____________。
(1)①2Cl-+2H2O  2OH-+Cl2↑+H2↑(3分)
2OH-+Cl2↑+H2↑(3分)
②Mg2++Ca(OH)2 = Mg(OH)2↓+ Ca2+ (3分)
(2)发出苍白色火焰(2分)
(3)BCA (2分)
(4)B>A>C(2分)
(5)3NaClO+CO(NH2)2=3NaCl+CO2↑+N2↑+2H2O
或NaOH+3NaClO+CO(NH2)2=3NaCl+NaHCO3+N2↑+2H2O
或2NaOH+3NaClO+CO(NH2)2=3NaCl+Na2CO3+N2↑+3H2O(3分)
【解析】
试题分析:(1)根据题给流程图知,反应①为电解饱和食盐水生成氢氧化钠、氢气和氯气,离子方程式为
2Cl-+2H2O  2OH-+Cl2↑+H2↑;反应②为镁离子和石灰乳的反应,离子方程式为
2OH-+Cl2↑+H2↑;反应②为镁离子和石灰乳的反应,离子方程式为
Mg2++Ca(OH)2 = Mg(OH)2↓+ Ca2+;(2)氯气在氢气中燃烧的实验现象:发出苍白色火焰;(3)粗盐中含有Ca2+、Mg2+、SO42-等杂质,可用过量氢氧化钡溶液除去镁离子和硫酸根,用过量碳酸钠溶液除去过量的钡离子和钙离子,过滤,用盐酸调节滤液的PH,精制时加入过量除杂试剂的正确顺序是BCA ;(4)设金属镁的物质的量为1mol,A.1mol镁在纯氧气(O2)中燃烧生成1mol氧化镁,质量为40g;B.1mol镁在二氧化碳气体中燃烧生成1mol氧化镁和0.5mol碳,质量为46g;C.1mol镁在空气中完全燃烧生成氧化镁和氮化镁的混合物,质量小于40g,得到的固体物质的质量由大到小的顺序是B>A>C;(5)NaClO与尿素CO(NH2)2的反应产物,通过实验发现产物除某种盐外,其余产物都是能参与大气循环的物质,则该反应的化学方程式为3NaClO+CO(NH2)2=3NaCl+CO2↑+N2↑+2H2O 。
考点:考查物质的分离提纯、方程式的书写及关系式法计算。

 阅读快车系列答案
阅读快车系列答案体积相同的甲、乙两份植物营养液,其所含组分的物质的量浓度如下表:
| KCl | K2SO4 | ZnCl2 | ZnSO4 |
甲 | 0.3 mol·L-1 | 0.2 mol·L-1 | 0 | 0.1 mol·L-1 |
乙 | 0.1 mol·L-1 | 0.3 mol·L-1 | 0.1 mol·L-1 | 0 |
下列对两份营养液成分的分析中,正确的是
A.两种溶液的n(Zn2+)不同
B.两种溶液的c(Cl-)之比为3:1
C.甲溶液的c(K+)=0.5 mol·L-1
D.两种溶液所含的N(SO42-)相等